已知,NA表示阿伏加德罗常数,下列有关说法正确的是 ( )
| A.11.2L NO气体中含有的原子总数为NA |
| B.1.0L 1.0mol·L-1的NaCl溶液中所含溶质的离子总数为NA |
| C.1mol 氦气体含有的电子总数为4NA |
| D.标准状况下,32gSO2气体所含的原子总数为1.5NA |
对于已达化学平衡的下列反应:2X(g)+Y(g) 2Z(g),减小压强时,对反应产生的影响是()
2Z(g),减小压强时,对反应产生的影响是()
| A.逆反应速率增大,正反应速率减小,平衡向逆反应方向移动 |
| B.逆反应速率减小,正反应速率增大,平衡向正反应方向移动 |
| C.正、逆反应速率都减小,平衡向逆反应方向移动 |
| D.正、逆反应速率都增大,平衡向正反应方向移动 |
可确认发生了化学平衡移动的是()
| A.化学反应速率发生了改变 |
| B.有气态物质参加的可逆反应达到平衡后,改变了压强 |
| C.由于某一条件的改变,使平衡混合物中各组分的浓度发生了不同程度的改变 |
| D.可逆反应达到平衡后,使用催化剂 |
已知工业上真空炼铷的原理如下:2RbCl+Ca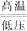 CaCl2+2Rb↑,对于此反应的进行能给予正确解释的是()
CaCl2+2Rb↑,对于此反应的进行能给予正确解释的是()
| A.铷的金属活动性不如钙强,故钙可置换铷 |
| B.铷的沸点比钙低,把铷蒸气抽出时,平衡右移 |
| C.该反应与金属活动顺序矛盾,该反应不能进行 |
| D.铷的单质比铷的化合物更稳定 |
在同一温度下将质量相同的N2O4和NO2分别充入体积相同的两个密闭容器a和b中,分别达到平衡后,结果是()
| A.a中N2O4的体积分数比b中高 | B.a中压强比b中小 |
| C.a中气体总物质的量比b中多 | D.a、b中各气体的体积分数相同 |
在某密闭容器中,可逆反应:A(g)+B(g) xC(g);ΔH<0符合图象(Ⅰ)所示关系。由此推断对图象(Ⅱ)的不正确说法是(p3>p4)()
xC(g);ΔH<0符合图象(Ⅰ)所示关系。由此推断对图象(Ⅱ)的不正确说法是(p3>p4)()
| A.Y轴表示A的转化率 | B.Y轴表示B的质量分数 |
| C.Y轴表示混合气体的密度 | D.Y轴表示混合气体的平均相对分子质量 |