从下列事实,不能用勒夏特列原理解释的是 ( )
A.在溴水中存在如下平衡:Br2+H2O  HBr+HBrO当加入NaOH溶液后颜色变浅 HBr+HBrO当加入NaOH溶液后颜色变浅 |
B.对   平衡体系增加压强使颜色变深 平衡体系增加压强使颜色变深 |
C.反应  CO2+NO△H<0升高温度使平衡向逆方向移动 CO2+NO△H<0升高温度使平衡向逆方向移动 |
D.合成氨反应: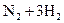   ,△H<0 为使氨的产率提高,理论上应采取低温高压的措施 ,△H<0 为使氨的产率提高,理论上应采取低温高压的措施 |
光盘是由二氧化硅玻璃材质制成.下列有关推断正确的是
A光盘遇水腐蚀 B光盘遇火会熔化
C光盘遇碱会腐蚀 D二氧化硅是导体
下列关于多环芳烃的推断不正确的是
| A.多环芳烃与苯互为同系物 |
| B.多环芳烃在一定条件下能与氢气发生加成反应 |
| C.多环芳烃是有毒物质,难溶于水 |
| D.下列一组多环芳烃中,碳的质量分数最大值为96% |

下列关于铅及其化合物描述不正确的是
| A.可溶性铅盐会导致人体蛋白质失去活性 |
| B.二氧化铅具有强氧化性 |
| C.为了方便,可以用新出版的报纸包裹熟食品 |
| D.推广使用无铅汽油,目的是降低空气中铅污染 |
下列有关锂的叙述正确的是
| A.锂在空气中燃烧生成过氧化锂 |
| B.根据对角线规则,锂与镁性质相似,蒸发、灼烧氯化锂溶液得到LiCl固体,电解该LiCl得到锂和氯气 |
| C.实验室锂保存在煤油中,防止锂与水、氧气反应 |
| D.“空中焰火”中既有物理变化又有化学变化 |
A、B、C分别是元素甲、乙、丙的单质,它们都是常见的金属或非金属,D、E、F是常见的三种氧化物,且有如图所示转化关系,则下列说法不正确的是
A.D、E中一定都含有A的元素
B.单质B肯定是氧化剂
C.A、B、C中一定有一种是氧元素的单质
D.若A是非金属,则B一定为金属