W、X、Y、Z均为短周期元素,W的最外层电子数与核外电子总数之比为7︰17;X与W 同主族;Y的原子序数是W和X的原子序数之和的一半;含Z元素的物质焰色反应为黄色。下列判断正确的是
同主族;Y的原子序数是W和X的原子序数之和的一半;含Z元素的物质焰色反应为黄色。下列判断正确的是
| A.金属性:Y>Z | B.氢化物的沸点:X<W |
| C.离子的还原性:X<W | D.原子及离子半径:Z>Y>X |
已知RO32-的R原子核内有x个中子,R的质量数为A,则m g RO32-含有电子的物质的量为
A. mol mol |
B.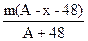 mol mol |
C. mol mol |
D. mol mol |
下列分子中所有原子都满足最外层8电子结构的是
① CO2,② CH4,③ PCl3,④ PCl5,⑤ BeCl2,⑥ N2[
| A.①④⑤ | B.①③⑥ | C.②④ | D.②③④⑤ |
科学家最近发现两种粒子:第一种是只由四个中子构成的粒子,这种粒子称为“四中子 ”,也有人称之为“零号元素”;第二种是由四个氮原子构成的分子。下列有关
”,也有人称之为“零号元素”;第二种是由四个氮原子构成的分子。下列有关 这两种粒子的说法不正确的是
这两种粒子的说法不正确的是
| A.“四中子” 粒子不显电性 | B.被称为零号元素是因为该粒子不含质子 |
| C.相同质量的N2和N4所含原子个数比为1∶2 | |
| D.第二种粒子的化学式为N4,与N2互为同素异形体 |
固体A的化学式为NH5,它的所有原子的最外层都符合相应稀有气体原子的最外电子层结构,则下列有关说法中,不正确的是
| A.1mol NH5中含有5 NA个N-H 键(NA表示阿伏伽德罗常数) |
| B.NH5中既有离子键又有共价键 |
| C.NH5的熔沸点高于NH3 |
| D.NH5固体投入水中的反应方程式是:NH4H+H2O=NH3·H2O+H2↑ |
下列排列顺序正确的是
①热稳定性:H2O>HF>H2S②原子半径:Na>Mg>O
③酸性:H3PO4>H2SO4>HClO4④物质的熔点 :石英>食盐>冰
:石英>食盐>冰
| A.①③ | B.②④ | C.①④ | D.②③ |