下列方法中可以说明2HI(g) H2(g)+I2(g)已达到平衡的是( )
H2(g)+I2(g)已达到平衡的是( )
①单位时间内生成n mol H2的同时生成n mol HI
②一个H—H键断裂的同时有两个H—I键断裂
③百分组成w(HI)=w(I2)
④反应速率v(H2)=v(I2)=1/2v(HI)时
⑤c(HI)∶c(H2)∶c(I2)=2∶1∶1时
⑥温度和体积一定时,容器内压强不再变化
⑦温度和体积一定时,某一生成物浓度不再变化
⑧条件一定,混合气体的平均相对分子质量不再变化
⑨温度和体积一定时,混合气体的颜色不再变化
⑩温度和压强一定时,混合气体的密度不再变化
| A.②③⑤ | B.①④⑦ | C.②⑦⑨ | D.⑧⑨⑩ |
胡椒酚是植物挥发油中的一种成分,关于胡椒酚的下列说法,其中正确的是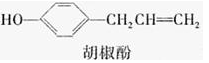
①该化合物属于芳香烃;
②分子中最多有7个碳原子处于同一平面;
③它的部分同分异构体能发生银镜反应;
④l 该化合物最多可与2
该化合物最多可与2
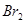 发生反应
发生反应
| A.①③ | B.①②④ | C.②③④ | D.②③ |
l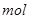 某气态烃最多可与2
某气态烃最多可与2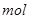
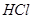 发生加成反应,所得产物与
发生加成反应,所得产物与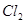 发生取代反应时,若将氢原子全部取代,需要6
发生取代反应时,若将氢原子全部取代,需要6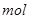
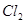 ,由此可知该烃结构简式可能为
,由此可知该烃结构简式可能为
A.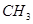 —CH━CH一 —CH━CH一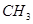 |
B.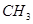 —C —C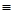 CH CH |
C.CH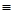 CH CH |
D.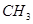 —C —C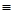 C—CH C—CH |
下列各组有机物,不管它们以何种比例混合,只要总质量一定,则完全燃烧时消耗氧气为一定值的是
A.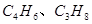 |
B.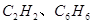 |
C.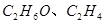 |
D.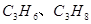 |
向淀粉中加入少量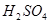 ,并加热使之水解。为测定淀粉的水解程度,所需下列试剂最恰当的组合是
,并加热使之水解。为测定淀粉的水解程度,所需下列试剂最恰当的组合是
①NaOH溶液 ②银氨溶液③新制的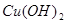 ④碘水⑤
④碘水⑤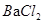 溶液
溶液
| A.①⑤ | B.②④ | C.①③④ | D.②③④ |
以2—氯丙烷为主要原料,制取1,2—丙二醇时,需要经过的反应先后分别为
| A.加成—消去—取代 | B.取代—加成—消去 |
| C.取代—消去—加成 | D.消去—加成—取代 |