某化学兴趣小组在探究常见物质转化时,发现部分物质存在如图所示的三角转化关系(部分反应物或生成物已略去)。已知①图中每个小三角形的三种物质中至少含有一种相同元素,K与L、A与B分别含有相同的元素。②D,J为固体单质,R为气体单质,其余为常见化合物。③A能使品红溶液褪色,也能使澄清石灰水变浑浊。④E为淡黄色化合物,E与C或L反应都能生成R。⑤I为氧化物,I与F或C都能反应;G和L反应生成难溶物H,H具有较强的吸附性。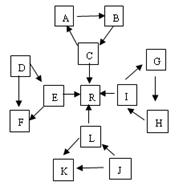
(1) J物质的化学式为 ,B所形成的晶体
为 晶体,工业上要让B转化为C,与B反应的原料是 。
(2)标况下,由E生成R 11.2 L时转移的电子数为 。
(3)C+J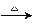 A+L的化学方程式为: 。
A+L的化学方程式为: 。
I+F→G的离子方程式为:  。
。
(4)常温下,测得一定浓度的G溶液的pH=10,试用离子方程式表示其原因 。
。
(5)J的最简单氢化物可与空气在碱性溶液中形成燃料电池,其负极电极反应式为 。
(6分)(1)P4(白磷,s)+5O2(g)=P4O10(s)ΔH=-2983.2kJ/mol
(2)P(红磷,s)+5/4O2(g)=1/4 P4O10(s)ΔH=-738.5kJ/mol
则白磷转化为红磷的热化学方程式为___________________。相同状况下,能量较低的是______;红磷的稳定性比白磷____
(10分)A~H是中学化学常见的物质,它们之间的转化关系如下图所示(部分产物已略去)。已知B、D是生活中常见的金属单质,G是气体单质,C的焰色反应呈黄色。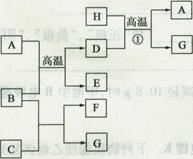

请回答下列问题:
(1)元素B在周期表中的位置是,C的电子式为,H的结构式为。
(2)反应①的化学方程式为。
(3)A与盐酸反应的离子方程式为。
(4)F溶液显(填“酸性”、“中性”或“碱性”),原因是(用离子方程式表示)。
(10分)某兴趣小组的同学用下图所示装置研究有关电化学的问题(甲、乙、丙三池中
溶质足量),当闭合该装置的电键K时,观察到电流计的指针发生了偏转。
请回答下列问题:
(1)甲池为(填“原电池”、“电解池”或“电镀池”),A电极的电极反应式为。
(2)丙池中F电极为(填“正极”、“负极”、“阴极”或“阳极”),该池的总反应
方程式为。
(3)当乙池中C极质量减轻10.8 g时,甲 池中B电极理论上消耗O2的体积为mL(标准状况)。
池中B电极理论上消耗O2的体积为mL(标准状况)。
(4)一段时间后,断开电键K。下列物质能使乙池恢复到反应前浓度的是(填选项字母)。
| A.Cu | B.CuO | C.Cu(OH)2 | D.Cu2(0H)2CO3 |
(12分)科学家一直致力于“人工固氮”的方法研究。
(1)合成氨的原理为:N2(g)+3H2(g) 2NH3(g)
2NH3(g) H=-92.4 kJ/mol,该反应的能量变化如图所示。
H=-92.4 kJ/mol,该反应的能量变化如图所示。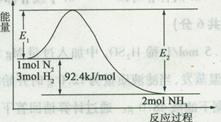
①在反应体系中加入催化剂,反应速率增大,E2的变化是(填“增大”、“减小”或“不变”)。
②将0.3 mol N2和0.5 mol H2充入体积不变的密闭容器中,在一定条件下达到平衡,测得容器内气体压强变为原来的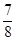 ,此时H2的转化率为;欲提高该容器中H2的转化率,下列措施可行的是(填选项字母)。
,此时H2的转化率为;欲提高该容器中H2的转化率,下列措施可行的是(填选项字母)。
| A.向容器中按原比例再充入原料气 | B.向容器中再充入一定量H2 |
| C.改变反应的催化剂 | D.液化生成物分离出氨 |
(2)根据最新“人工固氮”的研究报道,在常温、常压、光照条件下,N2在催化剂(掺有少量Fe2O3和TiO2)表面与水发生反应:
2N2(g)+6H2O(1) 4NH3(g)+3O2(g)
4NH3(g)+3O2(g) H="+1530" kJ/mol
H="+1530" kJ/mol
又知:H2O(1)=H2O(g) H=+44.0 kJ/mol
H=+44.0 kJ/mol
则2N2(g)+6H20(g) 4NH3(g)+302(g)
4NH3(g)+302(g) H =kJ/mol,该反应的化学平衡常数表达式为K=,控制其他条件不变,增大压强,K值(填“增大”、“减小”或“不变”)。
H =kJ/mol,该反应的化学平衡常数表达式为K=,控制其他条件不变,增大压强,K值(填“增大”、“减小”或“不变”)。
【有机化学基础】
Ⅰ.对羟基肉桂酸是一种强效的导电材料,在液晶显示器工业中近年来研究广泛。其结构简式如图所示: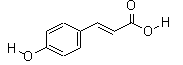
(1)该有机物具有的官能团名称是(写出其中的两种)
(2)该有机物能发生的反应类型是(填写代号)。
| A.酯化反应 | B.消去反应 | C.加成反应 | D.水解反应 |
Ⅱ.芳香族化合物C10H10O2有如下的转化关系:
已知E能使Br2/CCl4溶液褪色。请回答下列问题:
(3)请写出A的结构简式:。
(4)若有机物F与C互为同分异构体,则与有机物B互为同系物的F的同分异构体有
种。
(5)请写出B→C反应的化学反应方程式。