下列离子方程式书写正确的是
| A.向FeS中加入稀硝酸:FeS+2H+=Fe2++H2S↑ |
B.NH4HSO3溶液中加入足量的Na2O2固体:NH4++HSO3-+2OH- NH3+SO32-+2H2O NH3+SO32-+2H2O |
| C.(CN)2和Cl2的化学性质相似,将(CN)2通入KOH溶中:(CN)2+2OH-=CN-+CNO-+H2O |
| D.向Ba(NO)2溶液中通入CO2气体:Ba2++CO2+H2O=BaCO3↓+2H+ |
下列变化为放热的化学反应的是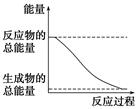
| A.H2O(g)===H2O(l) ΔH=-44.0 kJ·mol-1 |
| B.2HI(g)===H2(g)+I2(g) ΔH=+14.9 kJ·mol-1 |
| C.形成化学键时共放出862 kJ能量的化学反应 |
| D.能量变化如右图所示的化学反应 |
灰锡(以粉末状存在)和白锡是锡的两种同素异形体。
已知:
①Sn(白,s)+2HCl(aq)===SnCl2(aq)+H2(g) ΔH1
②Sn(灰,s)+2HCl(aq)===SnCl2(aq)+H2(g) ΔH2
③Sn(灰,s) 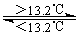 Sn(白,s)ΔH3=+2.1 kJ·mol-1
Sn(白,s)ΔH3=+2.1 kJ·mol-1
下列说法正确的是
| A.ΔH1>ΔH2 |
| B.锡在常温下以灰锡状态存在 |
| C.灰锡转化为白锡的反应是放热反应 |
| D.锡制器皿长期处在低于13.2 ℃的环境中,会自行毁坏 |
已知298 K时,合成氨反应N2(g)+3H2(g)  2NH3(g) ΔH=-92.0 kJ·mol-1,将此温度下的1 mol N2和3 mol H2放在一密闭容器中,在催化剂存在时进行反应。测得反应放出的热量为(假定测量过程中没有能量损失)
2NH3(g) ΔH=-92.0 kJ·mol-1,将此温度下的1 mol N2和3 mol H2放在一密闭容器中,在催化剂存在时进行反应。测得反应放出的热量为(假定测量过程中没有能量损失)
| A.一定小于92.0 kJ | B.一定大于92.0 kJ |
| C.一定等于92.0 kJ | D.无法确定 |
在下列各说法中,正确的是
| A.ΔH>0表示放热反应,ΔH<0表示吸热反应 |
| B.热化学方程式中的化学计量数只表示物质的量,可以是分数 |
| C.1 mol H2SO4与1 mol Ba(OH)2反应生成BaSO4沉淀时放出的热叫做中和热 |
| D.1 mol H2与0.5 mol O2反应放出的热就是H2的燃烧热 |
A、B、C、D、E、F为短周期六种元素,原子序数依次增大,其中A与E同主族且能形成离子化合物EA,B与F同主族,E与F同周期。D的核电荷数是B的最外层电子数2倍,单质F是一种重要的半导体材料。则下列推断中不正确的是
A.由A、C、D三种元素组成的化合物可以是离子化合物
B.F与D形成的化合物熔点高,可以与某种酸反应
C.原子半径由大到小的顺序是:E>F>C>D
D.五种元素中最高价氧化物对应的水化物酸性最强的是D