镁、铁混合物13.4 g溶解在足量的稀硝酸中,完全反应得到还原产物只有6.72 L(标况下) NO,则向反应后的溶液中加人足量的NaOH溶液,可生成的沉淀质量为
| A.26.8 g | B.28.7 g | C.29.1 g | D.29.5g |
下图所示的家庭小实验中,主要发生物理变化的是
下列事实与胶体性质无关的是
| A.由肾功能衰竭等疾病引起的血液中毒,可利用血液透析进行治疗 |
| B.水泥厂和冶金厂常用高压直流电除去大量烟尘,减少对空气的污染 |
| C.明矾可用作净水剂 |
| D.臭氧、Cl2均可用于水的消毒净化 |
表中关于物质分类的正确组合是
| 类别 组合 |
酸性氧化物 |
碱性氧化物 |
酸 |
碱 |
盐 |
| A |
CO2 |
SiO2 |
H2SO4 |
Na2CO3 |
NaHCO3 |
| B |
CO |
Na2O |
HCl |
NaOH |
NaCl |
| C |
SO2 |
Na2O2 |
CH3COOH |
KOH |
CaF2 |
| D |
SO3 |
CaO |
HNO3 |
Ca(OH)2 |
CaCO3 |
在t ℃时,将a g NH3完全溶于水,得到V mL溶液,假设该溶液的密度为ρ g/mL,质量分数为ω,其中含有NH4+的物质的量是b mol,下列叙述正确的是
A.溶质的质量分数ω= ×100% ×100% |
B.溶质的物质的量浓度c=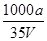 mo/L mo/L |
C.溶液中c(OH-)= mol/L+c(H+) mol/L+c(H+) |
| D.向上述溶液中加入V mL水,所得溶液的质量分数大于0.5ω |
配制0.1 mol/L的NaCl溶液,下列操作会导致所配溶液浓度偏高的是
| A.称量时,左盘高,右盘低 | B.定容时俯视读取刻度 |
| C.容量瓶洗净后未干燥 | D.定容时液面超过了刻度线 |