设NA为阿伏伽德罗常数,下列叙述正确的是: ( ) 
| A.18 g重水(D2O)中所含电子数为10 NA |
| B.在25 ℃,1.013×105 Pa条件下,11.2 L氯气所含原子数为 NA个 |
| C.常温常压下,32 g氧气中含有2 NA个氧原子 |
| D.32 g S8单质中含有的S—S键个数为12.04×1023 |
下列除去杂质的方法正确的是( )
| A.除去N2中的少量O2:通过灼热的CuO粉末,收集气体 |
| B.除去CO2中的少量HCl:通入Na2CO3溶液,收集气体 |
| C.除去FeCl2溶液中的少量FeCl3:加入足量铁屑,充分反应后,过滤 |
| D.除去KCl溶液中的少量MgCl2:加入适量NaOH溶液,过滤 |
甲、乙、丙、丁四种物质中,甲、乙、丙均含有相同的某种元素,它们之间具有如下转化关系: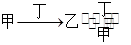 丙。下列有关物质的推断不正确的是()
丙。下列有关物质的推断不正确的是()
| A.若甲为焦炭,则丁可能是O2 |
| B.若甲为SO2,则丁可能是氨水 |
| C.若甲为Fe,则丁可能是盐酸 |
| D.若甲为NaOH溶液,则丁可能是CO2 |
下列推断合理的是( )
| A.在常温下,Na2SiO3+H2O+CO2=Na2CO3+H2SiO3↓,说明H2CO3酸性强于H2SiO3;在高温下,Na2CO3+SiO2= Na2SiO3+CO2↑,说明H2SiO3酸性强于H2CO3; |
| B.胶体区别于其他分散系的本质特点是能产生丁达尔现象 |
| C.KAl(SO4)2·12H2O是复盐;(NH4)2Fe(SO4)2也是复盐 |
| D.CaCl2、NaOH、HCl、HD四种物质都属于化合物 |
A~G各物质间的关系如下图所示,其中B、D为气体单质。则下列说法错误的是( )
A.若反应①在常温下进行,则1 mol A在反应中能转移1 mol电子
B.反应②的离子方程式为MnO2+4H++2ClˉMn2++2H2O+Cl2↑
C.新配制的F溶液一般需要加入铁屑和稀盐酸,前者用于防止Fe2+被空气氧化成Fe3+,后者可抑制Fe2+的水解
D.已知C的浓溶液在催化剂存在的条件下加热,能与B反应生成D,由此可以推断B的氧化性比MnO2强
下列关于物质的性质与应用相对应的是( )
| A.氯气有毒,不可用作自来水的杀菌消毒 |
| B.FeCl3溶液能与Cu反应,可用于蚀刻印刷电路 |
| C.硫粉具有还原性,可用于制造黑火药 |
| D.Na2O2具有强氧化性,可用作呼吸面具的供氧剂 |