下列离子方程式中正确的是 ( )
| A.用氯气作为水的消毒剂: Cl2+H2O = 2H++Cl-+ClO- |
B.向AlCl3溶液中加入过量氨水:Al3+ + 4NH3• H2O  AlO2-+ 4NH4+ + 2H2O AlO2-+ 4NH4+ + 2H2O |
| C.向Ba(OH)2溶液中滴加NaHSO4溶液至恰好为中性: Ba2+ + OH- + H+ + SO4  2-= BaSO4↓+ H2O 2-= BaSO4↓+ H2O |
| D.KI溶液与H2SO4酸化的H2O2溶液混合: 2 I- + H2O2 + 2 H+ ="2" H2O + I2 |
下列说法正确的是
A.同温同压下, 在光照和点燃条件下的 在光照和点燃条件下的 不同 不同 |
B.反应: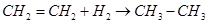 ; ; ,使用和未使用催化剂时,反应热不同 ,使用和未使用催化剂时,反应热不同 |
C.用硝酸这一种试剂就能将 、 、 、Na2CO3、 、Na2CO3、 四种溶液鉴别出来 四种溶液鉴别出来 |
| D.依据丁达尔现象就可将分散系分为溶液、胶体与浊液 |
下列有关化学用语表示正确的是
A.中子数为20的氯原子,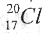 |
B.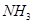 分子的电子式: 分子的电子式: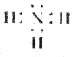 |
C.铝离子结构示意图: |
D.比例模型 表示甲烷分子或四氯化碳分子 表示甲烷分子或四氯化碳分子 |
生活中处处有化学,下列有关说法正确的是
| A.生活中常见的石英玻璃、普通玻璃、陶瓷都属于硅酸盐产品 |
| B.棉、麻、丝、毛、油脂都是天然有机高分子化合物 |
| C.白菜上洒少许福尔马林,既保鲜又消毒 |
| D.合金材料都是导体,可能含有非金属元素 |
有一混合物的水溶液,只可能含有以下离子中的若干种:K+、NH4+、Cl-、Mg2+、Ba2+、CO32-、SO42-,现取三份均为100mL溶液进行如下实验:
(1)第一份加入AgNO3溶液有沉淀产生
(2)第二份加足量NaOH溶液加热后,收集到气体0.04mol
(3)第三份加足量BaCl2溶液后,得干燥沉淀6.27g,经足量盐酸洗涤、干燥后,沉淀质量为2.33g。根据上述实验,以下推测正确的是()
| A.K+一定存在 | B.100mL溶液中含0.01mol CO32- |
| C.Cl-一定存在 | D.Ba2+一定不存在,Mg2+可能存在 |
在25℃、101kPa 下:①2Na(s)+1/2O2(g)=Na2O(s)△H1=-414KJ/mol
②2Na(s)+O2(g)=Na2O2(s)△H2=-511KJ/mol
下列说法正确的是()
| A.①和②产物的阴阳离子个数比不相等 |
| B.①和②生成等物质的量的产物,转移电子数不同 |
| C.常温下Na与足量O2反应生成Na2O,随温度升高生成Na2O的速率逐渐加快 |
| D.25℃、101kPa 下,Na2O2(s)+2 Na(s)= 2Na2O(s)△H=-317kJ/mol |