某化学课外小组设计了如下图(铁架台均已略去)所示的实验装置,进行气体性质实验。图中用箭头表示气体流向,A表示一种纯净、干燥的气体,B表示另一种气体。反应进行一段时间后,装置己中有红棕色气体生成。实验中所用的药品和干燥剂只能从下列物质中选取:Na2CO3、NaHCO3、MnO2、Na2O2、NaCl、无水CaCl2、NH4HCO3、碱石灰等固体和H2O2、蒸馏水。
根据图中装置和反应现象请回答:
(1)丙中发生反应的化学方程式为 。
(2)丁中的干燥剂应选 ,不选另一种干燥剂的理由是
。
(3)甲中发生反应的化学方程式为 。
(4)戊中发生的主要反应的化学方程式为 ,此反应是(吸热、放热) 反应,可能发生的什么现象可以证明你的判断 。
下图是某同学设计的木炭和浓硫酸反应并检验所得产物的实验装置。请回答:
⑴在装置①-④中,有明显错误的一个是(填编号)
⑵写出木炭和浓硫酸反应的化学方程式:。
如果有0.4mol电子转移,则在标准状况下产生气体L。
⑶无水硫酸铜的作用是
⑷装置①中所盛试剂是(填字母),装置④中所盛试剂是(填字母)。
A. 品红溶液 B. 澄清的石灰水 C. 酸性高锰酸钾溶液
(6分)下图表示配制100 mL 0.10 mol·L-1 Na2CO3溶液的几个关键实验步骤和操作,据图回答下列问题: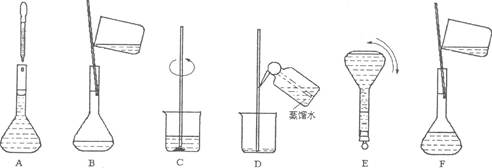
(1)步骤E中将一玻璃仪器上下颠倒数次,该仪器的名称是。
(2)步骤B通常称为转移,步骤A通常称为。
(3)将上述实验步骤A—F按实验过程先后次序排列。
(8分) 若用右图所示装置测定锌的相对原子质量,
实验步骤如下:
①称量ag纯锌放在铜网中,按图组装后,称得仪器和药品总质量为bg;
②将铜网浸入足量稀盐酸中,充分反应;
③反应完全后,称得仪器和药品总质量为cg。
请填空:
⑴产生H2的质量为----------g.
⑵ 锌的相对原子质量为----------.
⑶实验中碱石灰的作用是-----------------------------------------------,若去掉碱石灰,则测得的锌的相对原子质量-------------------..(偏大、偏小、无影响)
(共10分)已知氨可以与灼热的氧化铜反应得到氮气和金属铜,反应方程式为2NH3+3CuO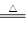 N2+3H2O+3Cu,用示意图中的装置可以实现该反应。回答下列问题:
N2+3H2O+3Cu,用示意图中的装置可以实现该反应。回答下列问题: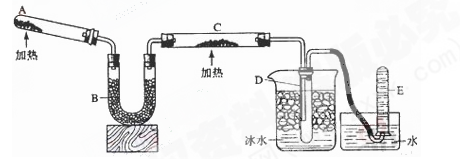
(1)A中发生反应的化学方程式是。检验氨气通常采用的方法及现象是_____________________,。
(2)B中加入的物质是,其作用是。
(3)实验时C中观察到的现象是,该反应中氨的作用是_______剂。
(4)若要检验反应生成的水,可将试管D及烧杯部分改成两个相连的干燥管,第一个干燥管X内装有_____________,现象是___________________;第二个干燥管Y内装有碱石灰,作用是____________________________。
某校化学兴趣小组为探究铁与浓硫酸反应,设计了图1、图2所示装置进行实验。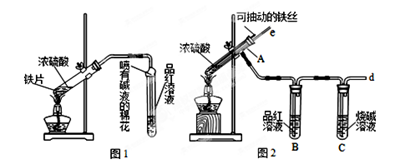
(1)比较两实验装置,图2装置的优点是:
①能更好的吸收有毒气体SO2,防止其污染环境;
②。
(2)导气管e有两个主要作用:一是在反应过程中,因导管插入液面下,可起到“液封”作用阻止SO2气体逸出而防止污染环境;二是。
(3)反应一段时间后,用滴管吸取A试管中的溶液滴入适量水中为试样,试样中所含金属离子的成分有以下三种可能:
Ⅰ:只含有Fe3+;Ⅱ:只含有Fe2+;Ⅲ:既有Fe3+又有Fe2+。
为验证Ⅲ的可能性,选用如下试剂,填写下列空格:
| A.稀HCl溶液 | B.稀H2SO4硫酸 | C.KSCN溶液 | D.KMnO4溶液 |
E.NaOH溶液 F.淀粉KI溶液 G.H2O2溶液
验证Ⅲ:步骤1.取试样,滴加少量的(填试剂序号),溶液的颜色变色,则试样中含有Fe3+。
步骤2.再取适量的试样滴加到少量的(填试剂序号),观察到的现象为,则试样中含有Fe2+。