有A、B、C、D、E五种短周期主族元素,其元素特征信息如下表:
| 元素编号 |
元素特征信息 |
| A |
其单质是密度最小的物质 |
| B |
阴离子带有两个单位的负电荷,单质是空气的主要成分之一 |
| C |
其阳离子与B的阴离子具有相同的电子层结构,且核电荷数与B相差 3 3 |
| D |
与C同周期,且最外层电子是C的3倍 |
| E |
与D同周期,原子半径在该周期中最小 |
请回答下列问题:
(1) 写出A、B、C三种元素形成的化合物的化学式为 。
(2) B、C、D的简单离子半径由大到小的顺序是(用离子符号表示) 。
(3 )写出电解CE溶液的化学方程式:
)写出电解CE溶液的化学方程式:
。( 本题共7分)
本题共7分)
氯化亚铜(CuCl)是白色粉末,不溶于水、乙醇,熔点422 ℃,沸点1366 ℃,在空气中迅速被氧化成绿色,常用作有机合成工业中的催化剂。以粗盐水(含Ca2+、Mg2+、SO42-等杂质)、Cu、稀硫酸、SO2等为原料合成CuCl的工艺如下: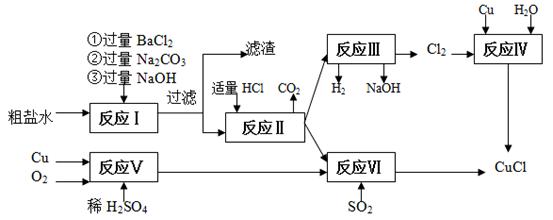
(1)在粗盐除杂的反应I中加Na2CO3溶液的作用是;
滤渣的主要成分:。
(2)反应Ⅱ完成后溶液中主要溶质是。
(3)反应IV和VI都是制备CuCl的化学过程:
①反应IV加入的Cu必须过量,其目的是。
②写出反应VI的离子方程式。
(4)反应VI后,过滤得到CuCl沉淀,用无水乙醇洗涤沉淀,在真空干燥机内于70 ℃干燥2小时,冷却,密封包装即得产品。于70℃真空干燥的目的是。
有一种节能的氯碱工业新工艺,将电解池与燃料电池相组合,相关流程如图所示(电极未标出):
回答下列有关问题:
(1)通入空气的电极为 (写电极名称)。燃料电池中阳离子的移动方向(“从左向右”或“从右向左”)。
(2)电解池中产生20 mol Cl2,理论上燃料电池中消耗mol O2。
(3)a、b、c的大小关系为:。
(4)以Al和NiO(OH)为电极,NaOH溶液为电解液组成一种新型电池,放电时NiO(OH)转化为Ni(OH)2,该电池放电时正极反应式是。
已知:A为常见的短周期轻金属,含A的合金材料常用于火箭、飞机等制造业;B是一种盐,在工农业生产中用途较广;C、F、H为常见非金属单质;常温下C、F、I、E、J和K为气体;E对空气的相对密度为0.586;常温常压下G为液体。有关物质间的转化关系如下(图中部分反应物或产物已省略):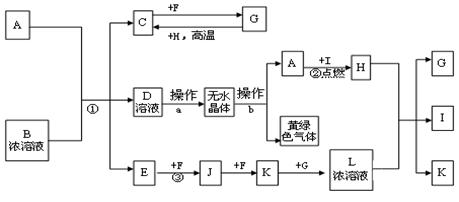
请填空:
(1)B的化学式为 。
(2)操作a必须在HCl气流中加热得无水物而不能直接加热浓缩,其原因是;操作b为 。
(3)反应①的离子反应方程式为。反应③的化学反应方程式为。
下表为元素周期表的一部分,请参照元素①-⑧在表中的位置,用化学用语回答下列问题:
| 族 周期 |
IA |
0 |
||||||
| 1 |
① |
ⅡA |
ⅢA |
ⅣA |
ⅤA |
ⅥA |
ⅦA |
|
| 2 |
② |
③ |
④ |
|||||
| 3 |
⑤ |
⑥ |
⑦ |
⑧ |
(1)④、⑤、⑥的离子半径由大到小的顺序为【用离子符号表示】。
(2)②、⑧、⑦的最高价含氧酸的酸性由强到弱的顺序是【用化学式表示】。
(3)①、④、⑤、⑧中的某些元素可形成既含离子键又含极性共价键的化合物,写出其中一种化合物的电子式:。
(4)由表中元素形成的常见物质X、Y、Z、M、N可发生以下反应:
X溶液与Y溶液反应的离子方程式为,N→⑥的单质的化学方程式为 。
高炉炼铁过程中发生的主要反应为1/3Fe2O3(s) + CO(g) 2/3Fe(s) + CO2(g)
2/3Fe(s) + CO2(g)
已知该反应在不同温度下的平衡常数如下:
请回答下列问题:
(1)该反应的平衡常数表达式K=_____________,△H________0(填“>”、“<”或“=”);
(2)在一个容积为10L的密闭容器中,1000℃时加入Fe、Fe2O3、CO、CO2各1.0 mol,反应经过l0 min达到平衡。求该时间范围内反应的平均反应速率υ(CO2)=" _________" 、CO的平衡转化率= _____________:
(3)欲提高(2)中CO的平衡转化率,可采取的措施是_____________。
| A.减少Fe的量 |
| B.增加Fe203的量 |
| C.移出部分CO2 |
| D.提高反应温度 |
E.减小容器的容积
F.加入合适的催化剂