相同物质的量的SO2和SO3相比较,下列叙述正确的是( )
①分子数之比为1:1 ②所含O原子数之比为2:3③原子总数之比为3:4 ④S原子数之比为1:1 ⑤质子数之比4:5
| A.①②③④⑤ | B.②③ | C.①⑤ | D.③④⑤ |
铜片、银片、Cu (NO3)2溶液、AgNO3溶液、导线和盐桥(装有琼脂-KNO3的U型管)构成一个原电池。以下有关该原电池的叙述正确的是
①实验过程中取出盐桥,原电池仍继续工作
②将铜片浸入AgNO3溶液中发生的化学反应与该原电池反应相同
③负极反应为:Ag+ + e- = Ag
④盐桥内的K+移向AgNO3溶液
| A.②④ | B.①② | C.②③ | D.③④ |
下列叙述中正确的是
| A.稀醋酸与稀氢氧化钠溶液发生中和反应的热化学方程式为 CH3COOH (aq) + NaOH (aq) = CH3COONa(aq) + H2O(l) ΔH = 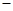 57.3kJ/mol 57.3kJ/mol |
| B.在101kPa时1mol物质燃烧时的反应热叫做该物质的燃烧热 |
| C.未来氢气作为新能源的其中一个优点是充分燃烧的产物不污染环境 |
| D.升高温度或加入催化剂,可以改变化学反应的反应热 |
在6KOH + 3Cl2 ="=" KClO3 + 5KCl + 3H2O的反应中,下列说法中正确的是
| A.KCl是还原产物,KClO3是氧化产物 |
| B.Cl2是氧化剂,KOH是还原剂 |
| C.KOH是氧化剂,Cl2是还原剂 |
| D.被氧化的氯原子与被还原的氯原子数之比为1∶5 |
有关纯碱和小苏打的叙述正确的是
| A.等质量的Na2CO3、NaHCO3分别与足量稀H2SO4反应,NaHCO3产生的CO2多 |
| B.等质量的Na2CO3、NaHCO3分别与足量的同种盐酸反应,NaHCO3消耗的盐酸多 |
| C.分别向NaHCO3和Na2CO3溶液中滴入Ba(OH)2溶液均出现白色沉淀 |
| D.Na2CO3和NaHCO3都既能与酸反应,又能与氢氧化钠反应 |
下列反应的离子方程式正确的是
| A.氢氧化钡溶液与稀硫酸反应:Ba2++ SO42- =BaSO4↓ |
| B.铝粉与稀硫酸反应:2Al +6H+=2Al3++3H2↑ |
| C.澄清石灰水与少量小苏打溶液混合:Ca2+十OH-+HCO3-= CaCO3↓+H2O |
| D.碳酸氢钠溶液中加入盐酸:CO32-+2H+ = H2O+CO2↑ |