将2 mol H2O和2 mol CO置于1 L容器中,在一定条件下,加热至高温,发生如下可逆反应:
2H2O(g) 2H2+O2、2CO+O2
2H2+O2、2CO+O2  2CO2。
2CO2。
(1)当上述系统达到平衡时,欲求其混合气体的平衡组成,则至少还需要知道两种气体的平衡浓度,但这两种气体不能同时是H2和H2O,或 和____(填它们的分子式)。
(2)若平衡时O2和CO2的物质的量分别为:n(O2)平=" " a mol, n(CO2)平=" b" mol。试求平衡时CO和H2O的物质的量:n(CO) = 、n(H2 O)= (用含a、b的代数式表示)。
甲醇是新型的汽车动力燃料。工业上可通过H2和CO化合制备甲醇,该反应的热化学方程式为:2H2(g)+CO(g) CH3OH(g)
CH3OH(g)
(1)已知: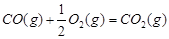
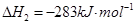
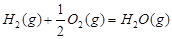

1 mol甲醇气体完全燃烧生成CO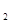 和水蒸气的热化学方程式为。
和水蒸气的热化学方程式为。
(2)下列措施中有利于提高2H2(g)+CO(g) CH3OH(g)反应速率的是(双选)。
CH3OH(g)反应速率的是(双选)。
| A.分离出CH3OH | B.升高温度 | C.减小压强 | D.加入合适的催化剂 |
(3)(3)用H2和CO化合制备甲醇的反应中,若反应的容积为1L的恒容容器,分别在230℃、250℃和270℃下,改变H2和CO的起始组成比(起始时CO的物质的量固定为1mol)进行实验,结果如下图所示(图中曲线上的点都为一定温度下、一定组成下的平衡点):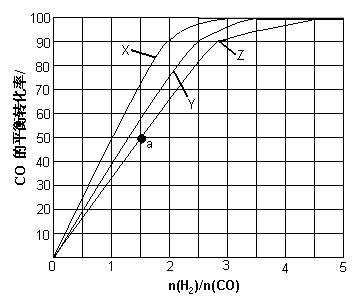
①曲线X对应的温度是。
②从图中可以得出的结论有(任写一条)。
(4)若往反应的容积中加入1.5molH2和1.0molCO,在曲线Z对应温度下反应达平衡。利用上述图中a点对应的CO平衡转化率,计算2H2(g)+CO(g) CH3OH(g)的平衡常数。(写出计算过程)
CH3OH(g)的平衡常数。(写出计算过程)
恒温条件下,将2.0molSO2与amolO2混合通入一密闭容器中,发生如下反应:2SO2(g)+O2(g) 2SO3(g)。反应达平衡时,测得容器内n(SO3)=1.3mol,n(O2)=3.0mol。
2SO3(g)。反应达平衡时,测得容器内n(SO3)=1.3mol,n(O2)=3.0mol。
求:⑴a的值。
⑵平衡时SO2的转化率。
将70 g过氧化钠和氧化钠的混合物跟98 g水充分反应后,所得氢氧化钠溶液的质量分数为50%。计算原混合物中过氧化钠和氧化钠的质量各为多少克?
将agNa溶于bg水中,a1gNa2O溶于b1g水中,a2gNa2O2溶于b2g水中,均得到溶质质量分数为8%的溶液.计算回答:
(1)当a1∶a2=31∶39时,则b1∶b2=__________.
(2)若a=4.6g,则b=__________g.
(1) 将铁片和铜片用导线连接并插入足量的CuSO4溶液中,当导线上有0.2mol电子通过时,从理论上分析铁片和铜片的质量变化(写出计算过程);
(2) 将(1)的反应中的铜片和导线去掉,也能发生反应,同样发生0.2mol电子转移时,铁片上的质量又如何变化?(简要地写出计算过程)