下列离子方程式书写可能正确的是 ( )
A.钠与水的反应:Na + H2O === Na+ +OH-+ H2↑  |
B.用浓盐酸与MnO2反应制取少量氯气:MnO2+2H++2Cl-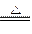 Mn2++Cl2↑+2H2O Mn2++Cl2↑+2H2O |
| C.在氢氧化钠溶液中通入少量的CO2:2OH- + CO2=CO32- + H2O |
| D.在硫酸铝溶液中加入过量氨水:Al3+ + 4OH- = AlO2-+2H2O |
以下化学反应的离子方程式书写正确的是( )
| A.硫酸与氢氧化钡溶液反应:H++OH-=H2O | B.碳酸钙与盐酸反应:CO32-+2H+=H2O+CO2↑ |
| C.铁与氯化铁溶液反应:Fe+Fe3+=2Fe2+ | D.氯气与溴化钠溶液反应:C12+2Br-=Br2+2Cl- |
下列说法不正确的是( )
| A.需要加热才能发生的反应是吸热反应 |
| B.燃料的燃烧反应都是放热反应 |
| C.每个化学反应都伴随着能量的变化 |
| D.化学反应的能量变化与反应物的总能量、生成物的总能量有关 |
下列互为同位素的是( )
| A.Na和Na+ | B.35Cl 和37Cl | C.14N 和14C | D.O2和O3 |
.下列判断正确的是( )
| A.核电荷数:Al<Na | B.金属性:Na>Al |
| C.原子序数:Na>Cl | D.原子半径:Cl>Na |
下列物质中既含有共价键又含有离子键的是( )
| A.NaI | B.CaCl2 | C.NO2 | D.KNO3 |