洪灾过后,饮用水的消毒杀菌成为抑制大规模传染性疾病爆发的有效方法之一,漂白粉是常用的消毒剂。
(1) 工业上将氯气通入石灰乳[Ca(OH)2]制取漂白粉,化学反应方程式为 。
(2)漂白粉的有效成分是(填化学式) 。
(3)漂白粉溶于水后,受空气中的CO2作用,即产生有漂白、杀菌作用的次氯酸,化学反应方程式为 。
(4)过氧化钠是 的固体,它与水和二氧化碳反应的化学方程式依次为 ; 因此,过氧化钠可作为 和 里氧气的来源(各1分)
2 )用20g烧碱配制成500mL溶液,其物质的量浓度,为 mol/L;从中取出1mL,其物质的量浓度为 mol/L;若将这1mL溶液用水稀释到100mL,所得溶液中溶质的物质的量浓度为 mol/L。
下图为常温下向25mL 0.1 mol·L-1 MOH溶液中逐滴滴加0.2 mol·L-1HA溶液过程中溶液pH的变化曲线。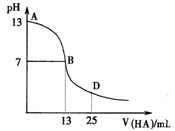
回答下列问题:
(1)上图能确定MOH为(“强”或“弱”)碱,
理由是。
(2)上图能确定HA为(“强”或“弱”)酸,
理由是。
(3)在D点时,溶液中c(A-)+c(HA)2c(M+)。(填“>”、“<”或“=”)
在100℃和200kPa的条件下,反应aA(g) bB(g)+c C(g)建立平衡后,在不加入任何物质的条件下逐步增大体系的压强(维护温度不变),下表列出的不同压强下反应建立平衡时物质B的浓度。
bB(g)+c C(g)建立平衡后,在不加入任何物质的条件下逐步增大体系的压强(维护温度不变),下表列出的不同压强下反应建立平衡时物质B的浓度。
| 压强(kPa) |
200 |
500 |
1000 |
| B的浓度(mol/L) |
0.04 |
0.1 |
0.27 |
根据表中的数据,回答下列问题:
(1)压强从200kPa增加到500kPa时,平衡移动(填“正向”或“逆向”或“不”),理由是。
(2)压强从500kPa增加到1000kPa时,平衡移动(填“正向”或“逆向”或“不”),其原因可能为。
把氯气通入稀氨水中,NH3分子上的一个H被Cl取代生成氯氨,然后加入过量的氨和氯氨作用,得到 联氨(N2H4)。
联氨(N2H4)。
(1)写出上述反应的化学方程式:________ __________
(2)联氨是一种可燃性液体,可用作火箭燃料。已知32.0g N2H4和H2O2反应生成氮气和水(气态),放出热量642kJ,该反应的热化学方程式是:
____________________________________________
(3)联氨的水溶液显弱碱性,用离子方程式表示其显弱碱性的原因:
_______________________________________________
(4)联氨—空气燃料电池是一种碱性燃料电池,电解质溶液是20%—30%的KOH溶液。联氨—空气燃料电池放电生成N2和H2O,其电极反应式是:正极________________________;负极_____________________。
下表是A、B、C、D、E五种有机物的有关信息;
 根据表中信息回答下列问题:
根据表中信息回答下列问题:
(1)A与溴的四氯化碳溶液反应的生成物的名称叫做;写出在一定条件下,A生成高分子化合物的化学反应方程式_______。
(2) A与氢气发生加成反应后生成分子F,F在分子组成和结构上相似的有机物有一大类(俗称“同系物”),它们均符合通式CnH2n+2。当n=__________时,这类有机物开始出现同分异构体。
(3) B具有的性质是(填号):①无色无味液体、②有毒、③不溶于水、④密度比水大、⑤与酸性KMnO4溶液和溴水反应褪色、⑥任何条件下不与氢气反应;写出在浓硫酸作用下,B与浓硝酸反应的化学方程式:。
(4) E反应能生成(C3H4O2)n的物质,该反应类型为 ;工业生产中使用镍作催化剂。但要求原料中含硫量小于5×10
;工业生产中使用镍作催化剂。但要求原料中含硫量小于5×10
 %,其目的是。
%,其目的是。
(5) 写出由C氧化生成D的化学反应方程式:。
(1)化合物A(C4H10O)是一种有机溶剂。A可以发生以下变化: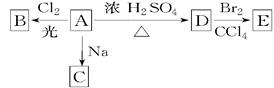
①A分子中的官能团名称是____________;
②A只有一种一氯取代物B,写出由A转化为B的化学方程式:________________________________________________________________________;
③A的同分异构体F也可以有框图内A的各种变化,且F的一氯取代物有三种,F的结构简式是
______________________________________。
(2)化合物“HQ”(C6H6O2)可用作显影剂,“HQ”可以与三氯化铁溶液发生显色反应。“HQ”还能发生的反应是(选填序号)____________________。
①加成反应 ②氧化 反应 ③加聚反应 ④水解反应
反应 ③加聚反应 ④水解反应
“HQ”的一硝基取代物只有一种。“HQ”的结构简式是______________________。
(3)A与“HQ”在一定条件下相互作用形成水与一种食品抗氧化剂“TBHQ”。“TBHQ”与氢氧化钠溶液作用得到分子式为C10H12O2Na2的化合物。
“TBHQ”的结构简式是____________________。