某反应中反应物与生成物有: 、
、 、
、 、
、 、
、 、Br2和。
、Br2和。
(1)配平上述化学反应方程式并标出电子转移的方向和数目: +
+ +
+  →
→  + Br2 +
+ Br2 +  + H2O
+ H2O
(2)反应中,被还原的元素是 ,还原剂是 。
(3)根据上述反应可推知 。
a.氧化性: b.氧化性:
b.氧化性:
c.还原性: >Br2 d.还原性:
>Br2 d.还原性: > Br2
> Br2
有原子序数依次增大的A、B、C、D、E五种元素,A是短周期中族序数等于周期数的非金属元素;B元素的原子既不易失去也不易得到电子,其基态原子中每种能级电子数相同;C元素的价电子构型为nsnnpn+1;D的最外层电子数与电子层数之比为3:1;E是地壳中含量仅次于铝的金属元素,其合金用途最广,用量最大。
(1)E元素在周期表中的位置;E元素价电子排布式为。
(2)A分别与B、C、D能形成电子数为10的化合物,它们的沸点由高到低的顺序是(写分子式)。
(3)B与D形成的非极性分子的电子式为________。
(4)B、C、D三种元素的第一电离能由大到小的顺序是____________(用元素符号表示)。
(5)C的单质分子中σ键和π键的个数比为________。
(6)已知在25℃、101kPa下:ABC(aq)+A2D(1)BC-(aq)+A3D+(aq) ΔH=+45.6kJ·mol-1
A3D+(aq)+DA-(aq)=2A2D(1)ΔH=-57.3kJ·mol-1
则在25℃、101kPa的稀溶液中,ABC与DA-反应的热化学方程式是(以离子方程式表示):。
NaHSO3可被过量KIO3氧化,当NaHSO3完全消耗时即有I2析出。某课题组用淀粉作指示剂,通过测定溶液变蓝所用时间来探究影响化学反应速率的因素。
(1)写出NaHSO3溶液与过量KIO3溶液反应生成I2的离子方程式:。
(2)调节反应物浓度和温度进行对比实验,记录结果如下:
| 编号 |
0.02mol/LNaHSO3溶液/mL |
0.02mol/LKIO3溶液/mL |
H2O/mL |
反应温度/℃ |
溶液变蓝的时间t/s |
| ① |
10 |
15 |
a |
10 |
t1 |
| ② |
10 |
40 |
0 |
10 |
t2 |
| ③ |
10 |
b |
0 |
20 |
t3 |
表中a=,b=。
(3)改变反应温度,重复实验③,得到温度(T)与溶液变蓝所需时间(t)的关系如下图所示(“×××”表示超过50℃后溶液不会再变蓝)。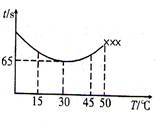
①在30℃下,若溶液变蓝时,I2的物质的量为n mol,则从反应开始至溶液变蓝,IO3-的平均反应
速率mol·L-1·s-1(写出表达式即可,不要化简)。
②根据图像,请你分析温度低于50℃时,溶液变蓝所需时间与反应温度的关系:。
(4)将NaHSO3溶液与KIO3溶液混合(预先加入可溶性淀粉为指示剂),用速率检测仪检测出起始阶段反应速率逐渐增大,一段时间后反应速率又逐渐减小。课题组对起始阶段反应速率逐渐增大的原因提出如下假设,请你完成假设二:
假设一:反应生成的I2对反应起催化作用;
假设二:;
………………
(5)请你设计实验验证上述假设一,完成下表中内容(反应速率可用测速仪测定)。
| 实验方案(不要求写出具体操作过程) |
预期实验现象和结论 |
工业上可以利用含铝、铁、铜合金的废料获得的绿矾(FeSO4·7H2O)、胆矾等,甲同学设计的实验方案如下: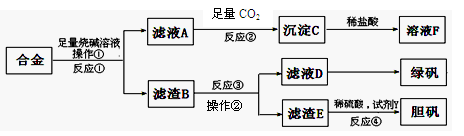
请回答:
(1)操作①、操作②所用的玻璃仪器是;沉淀C的化学式为。
(2)为了检测滤液D中含有的金属离子,可设计实验方案为(试剂自选)。
(3)在滤渣B中滴加稀硫酸时,发现反应速率比一般的铁粉反应要快,其原因是。
(4)若考虑绿色化学工艺,在滤渣E中加入稀硫酸和H2O2制胆矾晶体,则反应④的离子化学方程式为;若不考虑绿色化学工艺,所选试剂Y为1mol/L HNO3,欲使3mol Cu全部溶解且溶液中含铜元素的溶质仅为CuSO4,则需该硝酸的体积L。
邻羟基桂皮酸(D)是合成香精的重要原料,下列为合成邻羟基桂皮酸的路线之一
试回答:
(1)A中含氧官能团的名称是和。
(2)B→C的反应类型。
(3)D与过量NaOH溶液反应的化学方程式。
(4)有机物E与D互为同分异构体,且E有如下特点:
① 是苯的对位取代物, ② 能与NaHCO3反应放出气体 ,③能发生银镜反应。
请写出E的一种结构简式。
(5)下列说法正确的是。
a.A的化学式为C7H8O2b.B能与NaHCO3溶液反应
c.C可能发生聚合反应d.1mol有机物D最多能与4mol H2加成
Na、Cu、Fe、Cl、O、N是常见的6种元素。
(1)Fe位于元素周期表第_____周期第_____族;O的基态原子核外有______个未成对电子。
Cu的基态原子电子排布式为________。
(2)用“>”或“<”填空:
| 第一电离能 |
原子半径 |
稳定性 |
| N_______O |
Cl_______Na |
NH3______H2O |
(3)液态N2H4与液态N2O4反应生成气态水,在25℃、101kPa下,已知该反应每消耗1mol N2H4放出519.85kJ的热量,该反应的热化学反应方程式是:。
(4)古老的但仍是最有用的制备N2H4的方法是NaClO溶液氧化过量的NH3,写出该反应的离子方程式,并标出电子转移的方向和数目。