甲、乙两杯醋酸稀溶液,甲溶液的pH=a,乙溶液的pH=a+1,对下列叙述的判断正确的是 ( )
①甲由水电离出来的H+的物质的量浓度是乙的倍
②物质的量浓度c(甲)=10c(乙)
③中和等物质的量的NaOH溶液需甲、乙两杯酸的体积,10 V(甲)>V(乙)
V(甲)>V(乙)
④甲中的c(OH-)为乙中的c(OH-)的10倍
| A.①②④正确 | B.①③正确 | C.②④正确 | D.只有①正确 |
下列各组中的离子,能在溶液中大量共存的是()
| A.H+、Ca2+、Cl-、CO32- | B.Na+、Mg2+、SO42-、OH- |
| C.K+、Na+、OH-、Cl- | D.Cu2+、Ba2+、Cl-、SO42- |
下列离子方程式中,正确的是()
| A.稀硫酸滴在铜片上:Cu + 2H+ = Cu2+ + H2↑ |
| B.氧化镁和稀盐酸混合:MgO +2H+ = Mg2+ + H2O |
| C.铜片插入硝酸银溶液中:Cu + Ag+ = Cu2+ + Ag |
| D.稀盐酸滴在石灰石上:CO32- + 2H+ = H2O + CO2↑ |
如图所示,在蒸发皿中放一小块钠,加热至熔化时,用玻璃棒蘸取少量无水CuSO4与熔化的钠接触,瞬间产生耀眼的火花,同时有红色物质生成。据此判断下列说法中不正确的是() 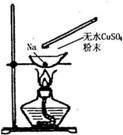
| A.上述反应是置换反应 |
| B.上述反应是放热反应 |
| C.上述反应中CuSO4表现了还原性 |
| D.加热且无水条件下,Na可以与CuSO4反应并生成Cu |
金属钠长期露置在空气中,最终生成的物质是()
| A.Na2O | B.NaOH | C.Na2CO3 | D.NaHCO3 |
下列物质中既能跟稀H2SO4反应, 又能跟氢氧化钠溶液反应的是 ()
①NaHCO3 ②Al2O3 ③Al(OH)3 ④Al
| A.③④ | B.②③④ | C.①③④ | D.全部 |