下列说法错误的是( )
| A.蒸发和蒸馏都是利用了混合物各组分沸点的不同 |
| B.食盐水的蒸发和自来水的蒸馏都能用到的仪器有铁架台、酒精灯、石棉网等 |
| C.分液时,将分液漏斗上口的玻璃塞打开的目的是为了平衡分液漏斗内外的气压,便于液体流下 |
| D.过滤时玻璃棒靠在三层滤纸一边 |
已知反应:FeO(s)+CO(g)= Fe(s)+CO2(g)的Kc=0.5(1273K)。若起始浓度c(CO)=0.05 mol/L,c(CO2)=0.01 mol·L-1,请回答:
(1)判断化学反应进行的方向并计算反应物、生成物的平衡浓度。
(2)CO的转化率是多少?
现有反应:mA(g)+nB(g) pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数减小,则:
pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数减小,则:
(1)该反应的逆反应为_________热反应,且m+n ________ p(填“>”、“=”或“<”)。
(2)减压时,A的质量分数________(填“增大”、“减小”或“不变”,下同)。
(3)若容积不变加入B,则A的转化率__________,B的转化率________。
(4)若升高温度,则平衡常数k将________。
(5)若加入催化剂,平衡时气体混合物的总物质的量_________。
(6)若B是有色物质,A、C均无色,则加入C(体积不变)时混合物颜色________;而维持容器内压强不变,充入氖气时,混合物颜色___________(填“变深”、“变浅”或“不变”)。
pH相等且等体积的醋酸和盐酸与足量的Zn反应,产生H2起始速率醋酸盐酸(填>,<或=),整个反应过程产生H2的平均反应速率醋酸盐酸(填>,<或=),放出的H2醋酸盐酸(填>,<或=);物质的量浓度相等,且等体积的醋酸和盐酸与足量的Zn反应,产生H2起始速率醋酸盐酸,放出H2的物质的量醋酸盐酸。
将6 mol A和5 mol B混合于4 L密闭容器中,发生如下反应:3A(g)+B(g) nC(g)+2D(g) 5 s后反应达到平衡状态,生成2 mol D,经测定以C表示的平均反应速率为0.1 mol·L-1·s-1。则下列结论中正确的是
nC(g)+2D(g) 5 s后反应达到平衡状态,生成2 mol D,经测定以C表示的平均反应速率为0.1 mol·L-1·s-1。则下列结论中正确的是
| A.以A表示的平均反应速率为0.1 mol·L-1·s-1 |
| B.平衡时,B的浓度为1 mol·L-1 |
| C.n值等于1 |
| D.平衡时B的转化率为50% |
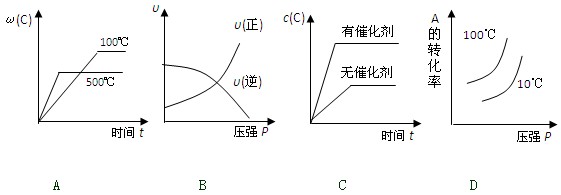
对于可逆反应:2A(g)+B(g)  2C(g);△H<0,下列各图正确的是
2C(g);△H<0,下列各图正确的是