下图是实验室制取Cl2并以Cl2为原料进行特定反应的实验: 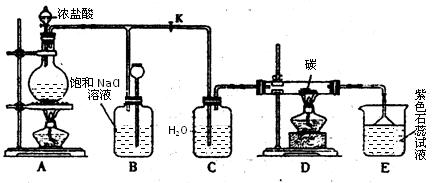
(1)A为氯气发生装置,写出反应的化学方程式________________________。
(2)实验开始先点燃A处的酒精灯,打开旋塞K,让Cl2充满整个装置,再点燃D处的酒精灯。Cl2通过C瓶后进入D,D装置内盛有碳粉,发生氧化还原反应,生成CO2和HCl,写出D装置中反应的化学方程式 _____;装置C的作用是 。
(3)E处石蕊试液的现象是_______________;其原因是__________________。
(4)若将E处溶液改为石灰水,反应过程的现象是_____________________________。
A.有白色沉淀生成
B.无白色沉淀生成
C.先生成白色沉淀,然后沉淀消失
(5)D处反应完毕后,关闭旋塞K,移去酒精灯,由于余热的作用,A处仍有少量Cl2产生,此处B中的现象是________________,B的作用是________________。
)某化学兴趣小组以含铁的废铝为原料制备硫酸铝晶体,设计如下的实验方案: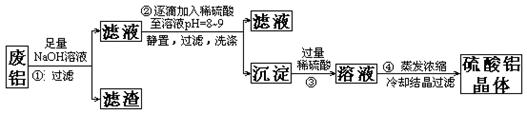
请回答以下问题:
(1)上述实验中多次用到过滤操作,该操作中要用到的玻璃仪器有;
(2)步骤②中有洗涤沉淀的操作,如何判断沉淀已洗涤干净:
;
(3)评价步骤②的操作中难以控制之处,请你提出一个合理而比较容易操作的实验方案(药品可任选)
;
(4)步骤①中使用的NaOH溶液以4mol/L为宜。某同学称量mgNaOH固体配制
V m L 4mol/L的NaOH溶液,下面是该同学配制过程的示意图,其操作中错误的是(填操作序号)。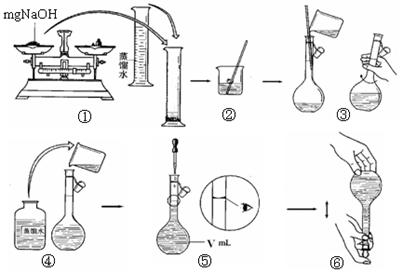
I.在足量的氯化亚铁溶液中加入少量(1—2滴)液溴,振荡后溶液变为黄色。
(1)甲同学认为是Br2单质溶于水变成黄色溶液;乙认为是Fe2+被氧化成Fe3+使溶液变成黄色。
(2)请根据提供试剂作出判断:
试剂: A 酸性高锰酸钾溶液 B 氢氧化钠溶液 C 四氯化碳 D 硫氰化钾溶液
判断: 两个同学的观点中正确的是__________(填 “甲” 或 “乙”), 并用两种方法(原理不同)加以试验证明, 写出选用的试剂编号及实验中观察到的现象:
| 选用试剂 |
实验现象 |
|
| 第一种方法 |
||
| 第二种方法 |
(3) 在FeCl3溶液中加入淀粉碘化钾溶液,能观察到的实验现象是。若选用淀粉碘化钾溶液来试验某观点的推断正确,你认为是否可行?;若可行本问不需要回答, 若不可行请说明原因: ________________________________________。
Ⅱ.若要把溶解于水中的Br2单质分离出来,所需要的主要玻璃仪器是_____, 该操作的名称是_ _
(Ⅰ)已知常温下苯酚微溶于水,溶解度为8.2g/100g水,其饱和溶液的物质的量浓度约为0.8mol/L。为了探究苯酚和乙醇分子中羟基上氢原子的活泼性,甲、乙两位同学分别设计了如下实验方案:
甲:向两只试管中,分别注入0.8mol/L的 乙醇和苯酚溶液3mL,各放入一小块金属钠,观察反应产生H2的速率。
乙醇和苯酚溶液3mL,各放入一小块金属钠,观察反应产生H2的速率。
乙:在两只试管中,分别放入1 g乙醇和苯酚晶体,各注入3mL蒸馏水,振荡,得到乙醇溶液和苯酚浊液,再向两试管中逐滴加入5mol/L的NaOH溶液,观察其中的变化。
(1)苯酚溶液与钠反应的离子方程式为_____________________________________。(2)对于甲、乙两个实验方案,他们能否达到实验目的?理由各是什么?
______________________________________________________________________。
(Ⅱ)在分析甲、乙两同学实验方案的基础上,丙同学进行了下列对比实验:
在两只试管中,分别放入2 g无水乙醇和苯酚晶体,用约60℃的水浴加热,待苯酚熔成液态后,再向两试管中各放入一小块金属钠。在乙醇中,钠块能与乙醇反应产生气体,约3min后钠块消失,溶液保持澄清;在苯酚中,钠块表面有少量气泡,约 2min后出现少量白色悬浮物,10min后白色悬浮物充满苯酚熔融液,振荡后发现钠块尚未完全消失。
2min后出现少量白色悬浮物,10min后白色悬浮物充满苯酚熔融液,振荡后发现钠块尚未完全消失。
(3)丙同学的实验表明,苯酚熔融液与钠的反应速率不如无水乙醇的快,其主要原因是____________________________________,因此苯酚熔融液和无水乙醇与钠反应的有关事实_________(填“能”或“不能”)作为判断分子里羟基上氢原子哪个更活泼的依据。 (4)请你设计一个探究苯酚和乙醇分子中羟基上氢原子活泼性的实验方案(可供选择的药品和仪器:乙醇、苯酚、蒸馏水、苯、钠、精确测
(4)请你设计一个探究苯酚和乙醇分子中羟基上氢原子活泼性的实验方案(可供选择的药品和仪器:乙醇、苯酚、蒸馏水、苯、钠、精确测 定溶液pH的仪器—pH计)
定溶液pH的仪器—pH计)
德国化学家李比希最早提出关于有机化合物中元素定量分析方法:用CuO作氧化剂(在氧气流中)将有机物氧化,再对产物进行分析,从而确 定有机物的实验式。现取m g某种氨基酸(CxHyOzNp)在纯氧中完全燃烧,生成CO2、H2O和N2。实验在下图装置中进行:
定有机物的实验式。现取m g某种氨基酸(CxHyOzNp)在纯氧中完全燃烧,生成CO2、H2O和N2。实验在下图装置中进行:
请回答下列问题:
(1)实验开始时,先要通一段时间的氧气,其理由是_____________________ ____________。
____________。
(2)装置图中需要加热的仪器有(用字母填空,下同)_________,操作时应先点燃________ 处的酒精灯。
处的酒精灯。
(3)A装置中发生反应的化学方程式是_________________________ _______________。
_______________。
(4)D装置的作用是_______________________________________________________。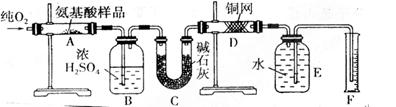
(5)读取N2的体积时,应注意:①_______________________________________;
②_____________________________________________________。
(6)实验中测得N2的体积为V mL(已折算成标准状况下)。为确定此氨基酸的分子式,还需要的有关数据有_______________。
| A.生成二氧化碳气体质量 | B.生成水的质量 |
| C.通入氧气的体积 | D.氨基酸的相对 分子质量 分子质量 |
为测定Na2CO3与Na2SO3混合物中各组分的含量,取样品23.2 g,用下图所示装置进行实验(铁架台、铁夹等仪器未在图中画出):
(1)将仪器连接好以后,必须进行的第一步操作是:___________________
(2)此实验还必须用到的最重要的仪器是_________________________;
仪器F的作用是____________________________________________。
(3)已知仪器C中装有品红溶液,其作用是_________________________。
(4)实验室中备有以下常用试剂:a.浓硫酸; b.品红溶液;c.酸性高锰酸钾溶液;d.饱和碳酸氢钠溶液;e.氢氧化钠溶液;f.无水硫酸铜;g.碱石灰;h.五氧化二磷;i.无水氯化钙。请将下列容器中应盛放的试剂序号填入相应空格:B中______,D中_________,E中__________。
(5)实验过程中,当仪器A内的固体反应完全后,需打开活塞K,向A中缓慢通入大量的空气。这样做的目的是__________________。所通空气应先经过___________试剂(填上述所供试剂的序号)处理,否则可能引起Na2SO3含量的测量结果比实际值_______________(填“偏高”、“偏低”或“没影响”)。
(6)若仪器E在实验完成时增重4.4 g,则Na2CO3与Na2SO3的物质的量之比为______。