(1)下列4组物质均有一种物质的类别与其它三种不同
A.CaO、Na2O、CO2、CuO B.H2、C、P、Cu
C.O2、Fe、Cu、Zn D.HCl、H2O、H2SO4、HNO3
以上四组物质中类别不同的物质依次是(填化学式)(各1分)
A ______;B __;C ;D 。
(2)写出下列物质在水溶液中的电离方程式:(各1分)
①氨水_________________________________________________________
②硫酸_________________________________________________________
③氢氧化钡_____________________________________________________
④硫酸铁_______________________________________________________
(3)将下列离子Na+、K+、Cu2+、H+、NO3-、Cl-、CO32-、OH-按可能大量共存于同一溶液的情况,把他们分成A、B两组,而且每组中均含两种阳离子和两种阴离子。(各2分)
A组: 。B组: 。
根据硫化氢气体的实验室制法和性质完成下列填空。
 (1)若用启普发生器制取硫化氢气体,则制取气体的原料可选用()。
(1)若用启普发生器制取硫化氢气体,则制取气体的原料可选用()。

| A. |
a.稀硫酸与硫化亚铁 b.稀硝酸与硫化亚铁 |

 (2)现要组装一套可以控制硫化氢气体产生速率的装置,请在图中选择合适的仪器;
(2)现要组装一套可以控制硫化氢气体产生速率的装置,请在图中选择合适的仪器;
 (填编号)。
(填编号)。



(3)如图,在一个充满氧气的集气瓶中加入少量品红稀硫溶液,
 点燃硫化氢气体。在火焰自动熄灭后,停止通入气体,瓶内可观察到
点燃硫化氢气体。在火焰自动熄灭后,停止通入气体,瓶内可观察到
 的现象是。
的现象是。


 (4)在上述集气瓶中继续通入硫化氢气体,振荡,发生反应的化学方程式为:
(4)在上述集气瓶中继续通入硫化氢气体,振荡,发生反应的化学方程式为:
 反应过程中,溶液的
(填"变大"、"变小"或"不变")。
反应过程中,溶液的
(填"变大"、"变小"或"不变")。
 (5)点燃不纯的硫化氢气体可能会发生爆炸,为了防止意外,可连接一个安全装置。如图的装置能起到此作用的是。
(5)点燃不纯的硫化氢气体可能会发生爆炸,为了防止意外,可连接一个安全装置。如图的装置能起到此作用的是。



 (6)已知硫化氢气体在空气中的体积分数为4.3%~45.5%时会发生爆炸。当硫化氢气体在空气中的体积分数为30%时,其爆炸产物是。
(6)已知硫化氢气体在空气中的体积分数为4.3%~45.5%时会发生爆炸。当硫化氢气体在空气中的体积分数为30%时,其爆炸产物是。
将一定量的
和含0.7
氧气的空气(忽略
)放入一定体积的密闭容器中,550℃时,在催化剂作用下发生反应:
 (正反应放热)。反应达到平衡后,将容器中的混合气体通过过量
溶液,气体体积减少了21.28
;再将剩余气体通过焦性没食子酸的碱性溶液吸收
,气体的体积又减少了5.6
(以上气体体积均为标准状况下的体积)。(计算结果保留一位小数)
(正反应放热)。反应达到平衡后,将容器中的混合气体通过过量
溶液,气体体积减少了21.28
;再将剩余气体通过焦性没食子酸的碱性溶液吸收
,气体的体积又减少了5.6
(以上气体体积均为标准状况下的体积)。(计算结果保留一位小数) 请回答下列问题:
请回答下列问题:



 (1)判断该反应达到平衡状态的标志是。(填字母)
(1)判断该反应达到平衡状态的标志是。(填字母) a.
和
浓度相等b.
百分含量保持不变
a.
和
浓度相等b.
百分含量保持不变 c.容器中气体的压强不变 d.
的生成速率与
的消耗速率相等
c.容器中气体的压强不变 d.
的生成速率与
的消耗速率相等 e.容器中混合气体的密度保持不变
e.容器中混合气体的密度保持不变 (2)欲提高
的转化率,下列措施可行的是(填字母)
(2)欲提高
的转化率,下列措施可行的是(填字母) a.向装置中再充入
b.向装置中再充入
a.向装置中再充入
b.向装置中再充入

c.改变反应的催化剂 d.生高温度 (3)求该反应达到平衡时
的转化率(用百分数表示)。
(3)求该反应达到平衡时
的转化率(用百分数表示)。 (4)若将平衡混合气体的5%通入过量的
溶液,生成沉淀多少克?
(4)若将平衡混合气体的5%通入过量的
溶液,生成沉淀多少克?
2SO2(g)+O2(g) =2SO3(g)反应过程的能量变化如图所示。已知1mol SO2(g)氧化为1mol SO3的ΔH=-99kJ·mol-1.请回答下列问题:
 (1)图中A、C分别表示 、 ,E的大小对该反应的反应热有无影响? 。该反应通常用V2O5作催化剂,加V2O5会使图中B点升高还是降低? ,理由是 ;
(1)图中A、C分别表示 、 ,E的大小对该反应的反应热有无影响? 。该反应通常用V2O5作催化剂,加V2O5会使图中B点升高还是降低? ,理由是 ;
 (2)图中△H= KJ·mol-1;
(2)图中△H= KJ·mol-1;
 (3)V2O5的催化循环机理可能为:V2O5氧化SO2时,自身被还原为四价钒化合物;四价钒化合物再被氧气氧化。写出该催化循环机理的化学方程式 ;
(3)V2O5的催化循环机理可能为:V2O5氧化SO2时,自身被还原为四价钒化合物;四价钒化合物再被氧气氧化。写出该催化循环机理的化学方程式 ;
 (4)如果反应速率υ(SO2)为0.05 mol·L-1·min-1,则υ(O2)= mol·L-1·min-1、υ(SO3)= mol·L-1·min-1;
(4)如果反应速率υ(SO2)为0.05 mol·L-1·min-1,则υ(O2)= mol·L-1·min-1、υ(SO3)= mol·L-1·min-1;
 (5)已知单质硫的燃烧热为296 KJ·mol-1,计算由S(s)生成3 molSO3(g)的△H (要求计算过程)。
(5)已知单质硫的燃烧热为296 KJ·mol-1,计算由S(s)生成3 molSO3(g)的△H (要求计算过程)。
浓H2SO4和木炭在加热时发生反应的化学方程式是




 2 H2SO4 (浓) + C
2 H2SO4 (浓) + C  CO2↑+ 2 H2O + 2SO2↑
CO2↑+ 2 H2O + 2SO2↑ 请从下图中选用所需的仪器(可重复选用)组成一套进行该反应并检出反应产物的装置。现提供浓H2SO4、木炭和酸性KMnO4溶液,其他固、液试剂自选。(连接和固定仪器用的玻
请从下图中选用所需的仪器(可重复选用)组成一套进行该反应并检出反应产物的装置。现提供浓H2SO4、木炭和酸性KMnO4溶液,其他固、液试剂自选。(连接和固定仪器用的玻
璃管、胶管、铁夹、铁架台及加热装置等均略去)
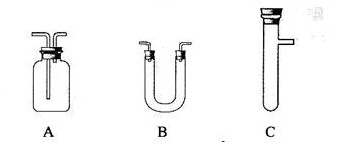
 将所选的仪器按连接顺序由上至下依次填入下表,并写出该仪器中应加试剂的名称及其作用。
将所选的仪器按连接顺序由上至下依次填入下表,并写出该仪器中应加试剂的名称及其作用。

选用的仪器 (填字母) (填字母) |
加入的试剂 |
作用 |
    |
下图表示某固态单质A及其化合物之间的转化关系(某些产物和反应条件已略去)。化合物B在常温常压下为气体,B和C的相对分子质量之比为4:5,化合物D是重要的工业原料。 (1)写出A在加热条件下与H2反应的化学方程式
(1)写出A在加热条件下与H2反应的化学方程式 _________________________________________________。
_________________________________________________。 (2)写出E与A的氢化物反应生成A的化学方程式 。
(2)写出E与A的氢化物反应生成A的化学方程式 。 (3)写出一个由D生成B的化学方程式 ______________________。
(3)写出一个由D生成B的化学方程式 ______________________。 (4)将5mL0.10mol·L-1的E溶液与10mL0.10 mol·L-1的NaOH溶液混合。
(4)将5mL0.10mol·L-1的E溶液与10mL0.10 mol·L-1的NaOH溶液混合。 ①写出反应的离子方程式________________________;
①写出反应的离子方程式________________________; ②反应后溶液的pH ______7(填“大于”、“小于”或“等于”),理由是________;
②反应后溶液的pH ______7(填“大于”、“小于”或“等于”),理由是________; ③加热反应后的溶液,其pH________(填“增大”、“不变”或“减小”),理由是________________________________。
③加热反应后的溶液,其pH________(填“增大”、“不变”或“减小”),理由是________________________________。