一定温度下的恒容容器中,能标志某可逆反应A(s)+2B(g) C(g)+D(g)已达平衡状态的是
C(g)+D(g)已达平衡状态的是
A.混合气体的压强不随时间变化而变化
B.气体总物质的量不随时间变化而变化
C. v (B)正=v (D)逆
D.单位时间内消耗n mol C,同时消耗2nmol B
往溴水加入苯后,振荡,静置,溴水层颜色变浅,这是由于()
| A.溴挥发出了 | B.发生了取代反应 |
| C.发生了加成反应 | D.发生了萃取 |
白酒、食醋、蔗糖、淀粉等均为家庭厨房中常用的物质,利用这些物质能完成下列实验的是()
①检验自来水中是否含氯离子 ②鉴别食盐和小苏打
③蛋壳能否溶于酸 ④白酒中是否含甲醇
| A.①② | B.①④ | C.②③ | D.③④ |
下列说法中错误的是()
| A.石油中含有C5~C11的烷烃,可以通过石油的分馏得到汽油 |
| B.含有16个碳以上的烷烃的重油经过催化裂化可以得到汽油 |
| C.煤是由有机物和无机物组成的复杂的混合物 |
| D.煤中含有苯和甲苯,可以用先干馏后分馏的方法把它们分离出来 |
下列说法正确的是()
| A.醇与酸的酯化反应的历程是酸脱氢,醇脱羟基 |
| B.乙醇具有消毒灭菌作用,越是浓的乙醇这样的作用越强 |
| C.任何一种酸与醇的作用都是酯化反应 |
| D.醇羟基不能与烧碱作用,而酚羟基能与烧碱作用,可以证明苯酚具酸性 |
下列物质与NaOH,Na2CO3,Cu(OH)2(新),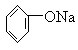 都能反应的是()
都能反应的是()
| A.乙醇 | B.乙醛 | C.甲酸 | D.乙醚 |