对于平衡体系 A(g)+
A(g)+ B(g)
B(g)
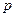 C(g)+
C(g)+ D(g) ΔH <0,下列结论中不正确的是
D(g) ΔH <0,下列结论中不正确的是
A.若温度不变,将容器的体积缩小到原来的一半,此时A的浓度为原来的2.1倍,则 +
+ <
<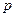 +
+
B.若平衡时,A、B的转化率相等,说明反应开始时,A、B的物质的量之比为 ∶
∶
C.若 +
+ =
=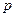 +
+ ,则往含有
,则往含有 mol气体的平衡体系中再加入
mol气体的平衡体系中再加入 mol的B,达到新平衡时,气体的总物质的量等于2
mol的B,达到新平衡时,气体的总物质的量等于2
D.若温度不变时,压强增大到原来的2倍,达到新平衡时,总体积一定比原来的1/2要小
下列说法不正确的是
| A.氢键在形成蛋白质二级结构和DNA双螺旋结构中起关键作用 |
| B.原子吸收光谱可用于测定物质中的金属元素,红外光谱可用于测定化合物的官能团 |
| C.阴极射线、a粒子散射实验及布朗运动发现都对原子模型建立做出了贡献 |
| D.常温常压下2g氦气含有的质子数与31g白磷中含有的P—P键数不一样多 |
常温时,将pH=6的CH3COOH溶液加水稀释1000倍后,溶液中的()
| A.pH=9 | B.c(OH-)≈10-5mol•L-1 |
| C.pH≈7 | D.c(OH-)≈10-8 mol•L-1 |
在一定温度不同压强(p1<p2)下,可逆反应2X(g) 2Y(g)+Z(g)中,生成物Z在反应混合物中的体积分数()与反应时间(t)的关系有以下图示,正确的是()
2Y(g)+Z(g)中,生成物Z在反应混合物中的体积分数()与反应时间(t)的关系有以下图示,正确的是()
下列说法正确的是()
| A.强电解质溶液的导电能力一定比弱电解质溶液的强 |
| B.氨气是弱电解质,铜是强电解质 |
| C.氧化钠是强电解质,醋酸是弱电解质 |
| D.硫酸钠是强电解质,硫酸钡是弱电解质 |
常温下测得某无色溶液中由水电离出的c(H+)为10-13mol•L-1,该溶液中一定能大量共存的离子组是()
| A.K+、Na+、NO3-、SO42- | B.K+、Na+、Cl-、CO32- |
| C.Mg2+、K+、NO3-、Cl- | D.Fe2+、NO3-、SO42-、NH4+ |