重铬酸钠(Na2Cr2O7)广泛用于合成颜料、媒染剂等,以铬铁矿(主要成分为Cr2O3,还有FeO、Al2O3、SiO2等杂质)为原料制取重铬酸钠的流程图如下:
请回答下列问题。
⑴铬铁矿中的Cr2O3与纯碱、O2在高温下反应的化学方程式为 ▲ 。
⑵若Ⅰ中只用一种试剂调节溶液的pH,应选用 ▲ (填标号)。
A.稀硫酸 B.氧化钠固体 C.氢氧化钾溶液
⑶Ⅰ中,调节溶液pH后,如果溶液的pH过小,可能导致W沉淀部分溶解,原因是:
▲ 。(用离子方程式表示)。
⑷Ⅱ中,Na2CrO4转化为Na2Cr2O7的离子反应如下:
2CrO42-(黄色)+2H+ Cr2O72-(橙红色)+H2O
Cr2O72-(橙红色)+H2O
①该反应 ▲ (填“是”或“不是”)氧化还原反应。
②若往Na2Cr2O7溶液(橙红色)中加入足量NaOH固体,溶液 ▲ (填标号)。
A.变黄色 B.颜色不变 C.橙红色变深
③已知:25℃,Ag2CrO4的Ksp=1.12×10-12,Ag2Cr2O7的Ksp=2×10-7。25℃,往Na2Cr2O7溶液中加入AgNO3溶液,最终只生成一种砖红色沉淀,该沉淀的化学式是 ▲ 。
(I)多项选择题
下列合成路线中,涉及到的反应类型有_________。
| A.加成反应 | B.氧化反应 | C.还原反应 |
| D.加聚反应 E.缩聚反应 |
(II)
(1)A的含氧官能团的名称是。
(2)A在催化剂作用可与H2反应生成B,该反应的反应类型是。
(3)酯类化合物C的分子式是C15H14O3,其结构简式是。
(4)A发生银镜反应的化学方程式是。
(5)扁桃酸( )有多种同分异构体。属于甲酸酯且含酚羟基的同分异
)有多种同分异构体。属于甲酸酯且含酚羟基的同分异
构体有种,写出 其中一个含亚甲基(-CH2-)的同分异构体的结构简式
其中一个含亚甲基(-CH2-)的同分异构体的结构简式
______________。
(6)N在NaOH溶液中发生水解反应的化学方程式是。
由A和其他无机原料合成环状化合物E,其合成过程如下:(水及其他无机产物均已省略)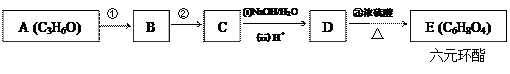
已知:RCH2Cl→RCH2OH,A的分子中不含甲基,且能使溴水褪色。试回答下列问题:
(1)写出结构简式:A__________________,D__________________;
(2)图中①的反应类型是_____________;
(3)写出反应③的化学方程式:________________________________________。
下图各物质是中学化学中常见的 物质,甲、乙均是离子化合物,且阴、阳离子个数比为1∶1。甲可作发酵粉,乙是一种常用的化肥。B、D常温下是气体。请回答下列问题:
物质,甲、乙均是离子化合物,且阴、阳离子个数比为1∶1。甲可作发酵粉,乙是一种常用的化肥。B、D常温下是气体。请回答下列问题:
(1)甲的俗名是________________。
(2)D的水溶液滴入酚酞试液后,溶液显红色,说明D溶液显____性,请用必要的文字加以解释并写出相关的离子方程式:____________。
(3)乙溶液与过量的KOH溶液共热,试写出反应的离子方程式:_____________。
我国对中药中重金属元素和有毒元素的含量等各项指标检查是非常严格的。下面是分析实验室对中草药中可能的 残余有毒元素As的检验方法和步骤(As在中草药中主要以As2O3的形式存在):
残余有毒元素As的检验方法和步骤(As在中草药中主要以As2O3的形式存在):
① 取1000g中草药样品进行前期处理制得待测溶液,此时样品中可能含有的As元素将转化为H3AsO3;
② 将待测溶液转移到250mL锥形瓶中,并加入2-3滴0.2%的淀粉溶液;
③ 用0.001mol/L标准碘溶液滴定待测溶液至终点,消耗20.00mL标准I2溶液,发生的反应为:H3AsO3+ I2+ H2O→H3AsO4+ I-+ H+(未配平)
试回答下列问题:
(1)简述如何对中草药样品进行前期处理制得待测溶液?。
(2)配平离子反应方程式:__H3AsO3+__I2+__H2O— __H3AsO4+__I-+__H+
(3)如何判断滴定到达终点?。
(4)我国《药用植物及制剂进出口绿色行业标准》中规定:绿色中药的砷含量不能超过
2.000mg/kg,试计算该草药样品中砷含量为mg/kg,则该草药样品(填
“合格”或“不合格”)。
A、B、C、D、E五种短周期元素,它们的原子序数依次增大。B原子的最外层电子数是其次外层电子数的2倍;C的最高价氧化物对应的水化物与其氢化物反应生成一种盐X;E与A同主族;A、B、C这三种元素中,每一种与D都能形成原子个数比不相同的若干种化合物。请回答下列问题:
(1)写出B的元素符号:__________。
(2)D在周期表中位于第__________周期,第__________纵行。
(3)C与E可形成离子化合物E3C,试写出它的电子式:__________。
(4)写出一个E和D形成的化合物与水反应的化学方程式:_______________________。
(5)盐X的水溶液显________(填“酸”“碱”或“中”)性,其原因用离子方程表示:_____________________________________。