将铁粉和硫粉混合后加热,待反应一发生即停止加热,反应仍可持续进行,直至反应完全生成新物质硫化亚铁。该现象说明了
| A.该反应是吸热反应 |
| B.铁粉和硫粉在常温下能自发反应 |
| C.该反应是放热反应 |
| D.生成物硫化亚铁的总能量高于反应物铁粉和硫粉的总能量 |
在实验室中,下列除杂的方法中正确的是()
| A.溴苯中混有溴,加入KI溶液,振荡,用汽油萃取出溴 |
| B.乙烷中混有乙烯,通入H2在一定条件下反应,使乙烯转化为乙烷 |
| C.硝基苯中混有浓硫酸和浓硝酸,将其倒入NaOH溶液中,静置,分液 |
| D.乙烯中混有CO2和SO2,将其通入NaOH溶液中洗气 |
下列物质中,既能因发生化学反应使溴水褪色,又能使酸性KMnO4溶液褪色的是()
①SO2②CH3CH2CH=CH2③ ④CH3CH3
④CH3CH3
| A.①②③④ | B.③④ |
| C.①②④ | D.①② |
以苯为原料,不能一步制得的物质是()
| A.环己烷 |
B.苯乙烯(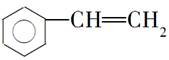 ) ) |
| C.溴苯 |
| D.硝基苯 |
对比饱和链烃、不饱和链烃的结构和性质,苯的独特性质具体来说是()
| A.难氧化,易加成,难取代 |
| B.易取代,能加成,难氧化 |
| C.易氧化,易加成,难取代 |
| D.因是单双键交替结构,故易加成为环己烷 |
苯乙烯是一种重要的有机化工原料,其结构简式为 ,它一般不可能具有的性质是()
,它一般不可能具有的性质是()
| A.易溶于水,不易溶于有机溶剂 |
| B.在空气中燃烧产生黑烟 |
| C.能使溴的四氯化碳溶液褪色,也能使酸性高锰酸钾溶液褪色 |
| D.能发生加成反应,在一定条件下可与4倍物质的量的氢气加成 |