下列关于热化学反应的描述中正确的是( )
| A.HCl和NaOH反应的中和热ΔH=-57.3kJ/mol,则H2SO4和Ca(OH) 2反应的中 和热△H=2×(-57.3)KJ/mol |
| B.CO(g)的燃烧热是283.0kJ/mol,则2CO2 (g)=2CO(g)+O2 (g)反应的 △H=+ 566.0kJ/mol |
| C.需要加热才能发生的反应一定是吸热反应 |
| D.1mol甲烷燃烧生成气态水和二氧化碳所放出的热量是甲烷的燃烧热 |
某强酸溶液pH=a,强碱溶液pH=b,已知a+b=12,酸碱溶液混合pH=7,则酸溶液体积V(酸)和碱溶液体积V(碱)的正确关系为()
| A.V(酸)=102V(碱) | B.V(碱)=102V(酸). |
| C.V(酸)=2V(碱) | D.V(碱)=2V(酸) |
pH=13的强碱溶液与pH=2的强酸溶液混合,所得溶液的pH=11,则强碱与强酸的体积比是().
| A.11∶1 | B.9∶1 | C.1∶11 | D.1∶9 |
pH=9的Ba(OH)2溶液与pH=12的KOH溶液,按4︰1的体积比混合,则混合溶液中H+浓度为(单位:mol·L-1)()
A.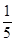 ×(4×10-9+1×10-12) ×(4×10-9+1×10-12) |
B.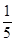 ×(8×10-9+1×10-12) ×(8×10-9+1×10-12) |
| C.5×10-10 | D.5×10-12 |
有人曾建议用AG表示溶液的酸度(acidity arede),AG的定义为AG=lg([H+]/[OH-])。下列表述正确的是()
| A.在25℃时,若溶液呈中性,则pH=7,AG=1 |
| B.在25℃时,若溶液呈酸性,则pH<7,AG<0 |
| C.在25℃时,岩溶液呈碱性,则pH>7,AG>0 |
| D.在25℃时,溶液的pH与AG的换算公式为AG=2(7-pH) |
某温度下,重水D2O的离子积为1.6×10-15,若用pH一样的定义来规定pD=-lgc(D+),以下关于pD的叙述正确的是()
| A.中性溶液的pD=7.0 |
| B.含0.01 mol的NaOD的D2O溶液1L,其pD=12.0 |
| C.溶解0.01 mol的DCl的D2O溶液1L,其pD=2.0 |
| D.在100 mL 0.25 mol·L-1的DCl重水溶液中,加入50 mL 0.2mol·L-1的NaOD的重水溶液,其pD=1.0 |