NA为阿伏加德罗常数,下列叙述中正确的是
①106 g Na2CO3晶体中的离子总数大于3NA
②标准状况下,16gO3和O2混合气体中含有的氧原子数为NA
③将0.1mol NaCl全部溶于乙醇中制成胶体,其中含有的胶体粒子数目为0.1NA
④1 mo1 N2和3 mol H2在一定条件下的密闭容器中充分反应,容器内的分子数大于2NA
| A.①② | B.②④ |
| C.①③ | D.③④ |
下列关于化学反应速率的说法中正确的是( )。
| A.化学反应速率可用某时刻生成物的物质的量来表示 |
| B.在同一反应中,用反应物或生成物表示的化学反应速率的值是相等的 |
| C.化学反应速率是指反应进行的时间内,反应物浓度的减少或生成物浓度的增加 |
| D.可用单位时间内氢离子物质的量浓度的变化来表示氢氧化钠和硫酸的反应速率 |
2012年6月16日18时37分24秒,神舟九号成功发射。飞船的能量部分来自太阳能电池,另外内部还配有高效的MCFC型燃料电池。该燃料电池可同时供应电和水蒸气,其所用燃料为氢气,电解质为熔融的碳酸钾。已知该燃料电池的总反应为2H2+O2=2H2O,负极反应为H2+CO32—-2e-=CO2↑+H2O,则下列推断正确的是( )。
| A.电池工作时,CO32—向负极移动 |
| B.电池放电时,电子经外电路由通氧气的正极流向通氢气的负极 |
| C.正极的电极反应为4OH--2e-=O2↑+2H2O |
| D.通氧气的电极为正极,发生氧化反应 |
实验室用铅蓄电池作电源电解饱和食盐水制取Cl2,已知铅蓄电池放电时发生如下反应:
负极:Pb+SO42—-2e-=PbSO4
正极:PbO2+4H++SO42—+2e-=PbSO4+2H2O
今欲制得Cl2 0.050 mol, 这时电池内消耗的H2SO4的物质的量至少是( )。
| A.0.025 mol | B.0.050 mol | C.0.10 mol | D.0.20 mol |
镁燃料电池具有比能量高、使用安全方便、原材料来源丰富、成本低、燃料易于贮运等特点。研究的燃料电池可分为镁—空气燃料电池,镁—海水燃料电池,镁—过氧化氢燃料电池,镁—次氯酸盐燃料电池。如图为镁—次氯酸盐燃料电池的工作原理图,下列有关说法不正确的是( )。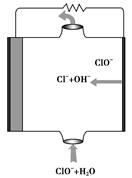
| A.放电过程中OH-移向正极 |
| B.电池的总反应式为Mg+ClO-+H2O=Mg(OH)2↓+Cl- |
| C.镁电池中镁均为负极,发生氧化反应 |
| D.镁—过氧化氢燃料电池,酸性电解质中正极反应为:H2O2+2H++2e-=2H2O |
如图为氢氧燃料电池示意图,按此图的提示,下列叙述不正确的是( )。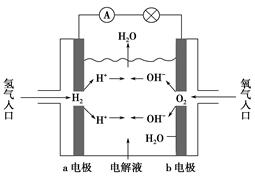
| A.a电极是负极 |
| B.b电极的电极反应为:4OH--4e-=2H2O+O2↑ |
| C.氢氧燃料电池是一种具有应用前景的绿色电源 |
| D.氢氧燃料电池是一种不需要将还原剂和氧化剂全部储藏在电池内的新型发电装置 |