为了除去粗盐中的Ca2+、Mg2+、 SO42-及泥沙,得到纯净的NaCl,可将粗盐溶于水,然后在下列操作中选取必要的步骤和正确的操作顺序:
SO42-及泥沙,得到纯净的NaCl,可将粗盐溶于水,然后在下列操作中选取必要的步骤和正确的操作顺序:
①过滤; ②加过量NaOH溶液; ③加适量盐酸;
④加过量Na2CO3溶液 ⑤加过量BaCl2溶液
| A.④②⑤ | B.④①②⑤③ | C.②⑤④①③ | D.①④②⑤ |
常温下将稀NaOH溶液与稀CH3COOH溶液混合,不可能出现的结果是()
| A.pH>7,且c(OH-)>c(Na+)>c(H+)>c(CH3COO-) |
| B.pH>7,且c(Na+)+c(H+)=c(OH-)+c(CH3COO-) |
| C.pH<7,且c(CH3COO-)>c(H+)>c(Na+)>c(OH-) |
| D.pH=7,且c(CH3COO-)>c(Na+)>c(H+)=c(OH-) |
物质的量浓度相同的下列溶液中,符合按pH由小到大顺序排列的是()
| A.Na2CO3NaHCO3NaClNH4Cl |
| B.Na2CO3NaHCO3NH4ClNaCl |
| C.(NH4)2SO4NH4ClNaNO3Na2S |
| D.NH4Cl(NH4)2SO4Na2SNaNO3 |
由一价离子组成的四种盐:AC、BD、AD、BC的1mol·L-1的溶液,在室温下前两种溶液的pH=7,第三种溶液pH>7,最后一种溶液pH<7,则()
| A |
B |
C |
D |
|
| 碱性 |
AOH>BOH |
AOH<BOH |
AOH>BOH |
AOH<BOH |
| 酸性 |
HC>HD |
HC>HD |
HC<HD |
HC<HD |
在常温下10mLpH=10的KOH溶液中,加入pH=4的一元酸HA溶液至pH刚好等于7(假设反应前后体积不变),则对反应后溶液的叙述正确的是()
| A.c(A-)=c(K+) |
| B.c(H+)=c(OH-)<c(K+)<c(A-) |
C.V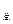 ≥20mL ≥20mL |
D.V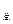 ≤20mL ≤20mL |
下列混合液中,各离子浓度的大小顺序正确的是()
| A.10mL0.1mol·L-1NH4Cl溶液与5mL0.2mol·L-1NaOH溶液混合,c(Na+)>c(Cl-)>c(OH-)>c(H+) |
B.10mL0.1mol·L-1氨水与10mL0.1mol·L-1盐酸混合,c(Cl-)>c(NH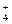 )>c(OH-)>c(H+) )>c(OH-)>c(H+) |
| C.10mL0.1mol·L-1CH3COOH溶液与5mL0.2moL·L-1NaOH溶液混合,c(Na+)>c(CH3COO-)>c(OH-)>c(H+) |
| D.10mL0.5mol·L-1CH3COONa溶液与6mL1mol·L-1盐酸混合,c(Cl-)>c(Na+)>c(OH-)>c(H+) |