漂白剂亚氯酸钠(NaClO2)在常温与黑暗处可保存一年。亚氯酸不稳定可分解,反应的离子方程式为:5HClO2 = 4ClO2↑+ H+ + Cl- + 2H2O。向NaClO2溶液中滴加H2SO4,开始反应缓慢,随后反应迅速,其原因是( )
| A.在酸性条件下亚氯酸的氧化性增强 | B.溶液中的H+起催化作用 |
C.ClO 2逸出,使反应的生成物浓度降低 2逸出,使反应的生成物浓度降低 |
D.溶液中的Cl-起催化作用 |
在25℃下,将a mol·L-1的CH3COONa与0.02 mol·L-1的盐酸等体积充分混合,反应后测得溶液pH=7,则:
(1)a0.02(填“<”、“>”或“=”);
(2)c(CH3COO-)+ c(CH3COOH)=mol·L-1,c(CH3COOH)=mol·L-1;
(3)CH3COOH的电离平衡常数Ka=(用含a的代数式表达)。
(4)反应后溶液中各种离子浓度由大到小顺序是
化学中常借助曲线图来表示某种变化过程,有人分别画出了下列的四个曲线图:
有关上述曲线图的说法正确的是:
| A.曲线图①可以表示恒压容器中某化学平衡体系充入气体生成物后反应速率随时间的变化 |
| B.曲线图②可以表示向一定量的氢氧化钠溶液中滴加一定浓度的盐酸时的pH的变化 |
| C.曲线图③可以表示向一定量的明矾溶液中滴加一定浓度的氢氧化钡溶液时的产生沉淀的物质的量变化 |
| D.曲线图④可以表示冰醋酸加水稀释过程中溶液中c(H+)的变化 |
下列各项所给的两个量,前者—定小于后者的是:
①纯水在25℃和80℃的pH;②1moINaHSO4和1mo1 Na2SO4在熔化状态下的离子数;
③25℃时,等体积且pH都等于3的盐酸和AlCl3的溶液中,已电离的水分子数;
④常温下,pH为10的氨水溶液和pH为12氨水溶液中所含溶质分子数。
| A.①② | B.②④ | C.①③ | D.②③ |
某密闭容器中充入等物质的量的A和B,一定温度下发生反应A(g)+xB(g)  2C(g),达到平衡后,在不同的时间段,分别改变影响反应的一个条件,测得容器中各物质的物质的量浓度、反应速率分别随时间的变化如下图所示:
2C(g),达到平衡后,在不同的时间段,分别改变影响反应的一个条件,测得容器中各物质的物质的量浓度、反应速率分别随时间的变化如下图所示: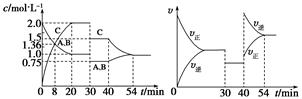
下列说法中正确的是
| A.30~40 min该反应使用了催化剂 |
| B.反应方程式中的x=1,正反应为吸热反应 |
| C.30 min时降低压强,40 min时升高温度 |
| D.8 min时反应第一次达到平衡 |
某温度下,pH相同的盐酸和氯化铵溶液分别稀释,pH随溶液体积变化的曲线如下图所示。据图判断下列叙述中,正确的是
| A.Ⅰ为氯化铵稀释时pH值变化曲线,Ⅱ为盐酸稀释时pH值变化曲线 |
| B.b点溶液中水的电离程度比d点溶液中水的电离程度大,但两点的KW相同 |
| C.a点时,等体积的两溶液分别与NaOH反应,消耗的NaOH量相同 |
| D.c点溶液的导电能力一定比b点溶液导电能力强 |