小刚、小军、小红对一久置的NaOH白色粉末的成分进行探究。
三位同学都作出以下的猜想:
Ⅰ.①可能是NaOH; ②可能是Na2CO3; ③可能是NaOH与Na2CO3的混合物。
做出②③猜想的依据是______________________________(用化学方程式表示)
Ⅱ.为了验证①②③猜想,他们分别做了下面的实验。
(1)小刚取少量白色粉末于试管中,再滴加稀HCl,有气泡产生,由此可推出白色粉末中一定含有 ,可肯定猜想________(填序号)是错误的。
(2)小军又取少量白色粉末溶于水,向所得溶液中滴加酚酞试液,溶液变为红色。由此小军结合小刚的实验,认为猜想③是正确的。小红却认为小军的所得结论不确切,因为
。
(3)为探究白色粉末是否含有NaOH,小红设计了如下实验方案: 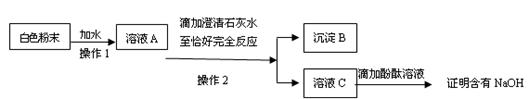
①沉淀B的化学式为____________。
②在操作1中要用到玻璃棒,其作用是_______________;
在操作2中,除要用到铁架台(带铁 圈)、烧杯、滤纸、玻璃棒外,还需补充的玻璃仪器是 _______。
圈)、烧杯、滤纸、玻璃棒外,还需补充的玻璃仪器是 _______。
③小刚认为小红的这个方案也有问题,理由是________________。
Ⅲ.小刚对小红的实验作了正确的改进后进行了 实验,实验现象和小红的一致。由此确定猜想③是正确的
实验,实验现象和小红的一致。由此确定猜想③是正确的 。小刚改进的方法是_______ 。
。小刚改进的方法是_______ 。
X、W、Y、Z分别代表原子序数依次减小的四种短周期元素,它们满足以下条件:X原子L层电子数是其最外层电子数的2倍;W原子K、L层电子数之和比L、M层电子数之和多1个电子;Y是地壳中含量最多的元素;Z是常见的非金属元素,其一种单质能够导电。请填空:
(1)X元素在元素周期表中的位置。原子结构示意图为。
(2)Y和Z组成的一种其原子个数比为2:1的化合物化学式:。
(3)W与Y可组成一种其原子个数比为1:1的化合物A,写出该化合物A的名称:;Y和Z组成的一种化合物B,写出该化合物B与化合物A反应的化学方程式。
某课外活动小组用如图装置进行实验,试回答下列问题。
(1)若开始时开关K与a连接,则B极的电极反应式为__________。
(2)若开始时开关K与b连接,则B极的电极反应式为____________,总反应的离子方程式为_________________________________。
(3)若开关K与b连接,下列说法正确的是(填序号)______________。
①溶液中Na+向A极移动
②从A极处逸出的气体能使湿润的KI淀粉试纸变蓝
③反应一段时间后加适量盐酸可恢复到电解前电解质的浓度
④若标准状况下B极产生2.24 L气体,则溶液中转移0.2 mol电子
(4)如果模拟工业上离子交换膜法制烧碱的方法,将制得的氢气、氧气和氢氧化钾溶液组合为氢氧燃料电池,则电池正极的电极反应式为。
(10分)为测定NaOH溶液的浓度,实验如下:用标准稀盐酸溶液进行滴定
(1)配制100 mL 0.1000mol·L-1盐酸标准溶液所需仪器除量筒、小烧杯、玻璃棒、胶头滴管外,还需要
(2)用量取20.00 mL待测NaOH溶液放入锥形瓶中,滴加2~3滴酚酞作指示剂,用标准盐酸溶液进行滴定。为减小实验误差,进行了三次实验,假设每次所取NaOH溶液体积均为20.00 mL,三次实验结果如下:
| 实验次数 |
第一次 |
第二次 |
第三次 |
| 消耗盐酸溶液体积/mL |
19.00 |
23.00 |
23.04 |
该NaOH溶液的浓度约为____________________
(3)滴定时边滴边摇动锥形瓶,眼睛 ______
(4)下列操作会造成测定结果(待测NaOH溶液浓度值)偏低的有_____
A.配制标准溶液定容时,加水超过刻度
B.锥形瓶水洗后直接装待测液
C.酸式滴定管水洗后未用标准稀盐酸溶液润洗
D.滴定到达终点时,俯视读出滴定管读数;
E.酸式滴定管尖嘴部分有气泡,滴定后消失
F.摇动锥形瓶时有少量液体溅出瓶外
某同学在用锌与稀硫酸反应制取氢气的实验中,发现加入少量硫酸铜溶液可加快氢气生成的速率。请回答下列问题:
(1)上述实验中,发生的化学反应方程式有______________________________
(2)硫酸铜溶液加快氢气生成的速率的原因______________________________
(3)实验室现有Na2SO4、MgSO4、HgSO4、K2SO4等四种溶液,可与上述实验中CuSO4溶液起相似作用的是____________________
(4)要加快上述实验中气体生成的速率,还可以采取的措施有____________
现有浓度均为0.1 mol·L 的下列溶液:①硫酸、②醋酸、③氢氧化钠、④氯化铵、⑤醋酸铵、⑥硫酸氢铵、⑦氨水,请回答下列问题:
的下列溶液:①硫酸、②醋酸、③氢氧化钠、④氯化铵、⑤醋酸铵、⑥硫酸氢铵、⑦氨水,请回答下列问题:
(1)①、②、③、④四种溶液中由水电离出的H 浓度由大到小的顺序是_____(填序号)。
浓度由大到小的顺序是_____(填序号)。
(2)④、⑤、⑥、⑦四种溶液中NH 浓度由大到小的顺序是_____(填序号)。
浓度由大到小的顺序是_____(填序号)。
(3)已知t℃时,K =1×10
=1×10 。现在t℃时将pH=11的NaOH溶液aL与pH=1的H2SO4溶液bL混合(忽略混合后溶液体积的变化),若所得混合溶液的pH=2,则a:b=_____。
。现在t℃时将pH=11的NaOH溶液aL与pH=1的H2SO4溶液bL混合(忽略混合后溶液体积的变化),若所得混合溶液的pH=2,则a:b=_____。