分类方法在化学学科的发展中起到重要的作用。下列分类标准合理的是
| A.根据纯净物的元素组成,将纯净物分为单质和化合物 |
| B.根据溶液导电能力强弱,将电解质分为强电解质、弱电解质 |
| C.根据是否具有丁达尔效应,将分散系分为溶液、浊液和胶体 |
| D.根据反应中的能量变化,将化学反应分为“化合、分解、复分解、置换”四类 |
下列物质结构与对应的用语表达都正确的是 ( )
| A.S-C-S:二硫化碳的结构式 | B.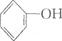 :苯酚的结构简式 :苯酚的结构简式 |
C.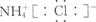 :氯化铵的电子式 :氯化铵的电子式 |
D.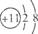 :钠离子的结构示意图 :钠离子的结构示意图 |
下列描述,其因果关系成立的是
| A.因为NH3的水溶液可以导电,所以NH3是电解质 |
| B.因为SO2可以使溴水褪色,所以SO2具有漂白性 |
| C.因为某碱性溶液的焰色呈黄色,所以其溶质为NaOH |
| D.因为电解质溶于水后电离为离子,所以电解质在溶液中的反应实质是离子反应 |
蒽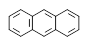 的一氯取代物其同分异构体的种类有
的一氯取代物其同分异构体的种类有
| A.2种 | B.3种 | C.4种 | D.5种 |
能正确表示下列化学反应的离子方程式是
| A.用氢氧化钠溶液吸收少量二氧化硫:2OH-+SO2=SO32-+H2O |
| B.金属铝溶于盐酸中:Al+2H+=Al3++H2↑ |
| C.硫酸铜溶液与氢氧化钡溶液反应:SO42-+Ba2+=BaSO4↓ |
| D.碳酸镁溶于硝酸中:CO32-+2H+=H2O+CO2↑ |
通过实验方法测得H2+Cl2 = 2HCl的化学反应速率v和反应物浓度c的关系式为:
v =" k" ·c(H2)m ·c(Cl2)n。式中k为常数,m、n的数值可用下表中数据确定。
| c(H2) / mol·L-1 |
1.0 |
2.0 |
2.0 |
| c(Cl2) / mol·L-1 |
1.0 |
1.0 |
4.0 |
| v / mol·L-1·s-1 |
1.0 k |
2.0 k |
4.0 k |
由此可推得,m、n值正确的是
A.m=1,n=1 B.m=1/2,n=1/2C.m=1/2,n=1 D.m=1,n= 1/2