Ⅰ.下列有关实验操作或结果的说法中正确的是 (填字母)
| A.滴定时,眼睛应始终注视滴定管内液面的变化 |
| B.用碱式滴定管量取0.10 mol·L-1的KMnO4溶液15.10 mL |
| C.酸碱中和滴定之前,锥形瓶用蒸馏水洗净即可,不能用待测液润洗 |
| D.用pH试纸测量某溶液的pH时要先将试纸润湿 |
E.滴定管经蒸馏水洗净后,直接注入标准液,将使测得的待测液浓度偏高
F.用广泛pH试纸测量H2SO4溶液的pH时,测得pH=3.2
G.测定酸碱滴定曲线:开始时测试和记录的间隔可稍小些,滴定至终点附近则要大些
Ⅱ.(1)由氢气和氧气反应生成1 mol水蒸气放热241.8kJ,写出该反应的热化学方程式 。已知H2O(l) = H2O(g) ΔH =+44 kJ·mol-1则标准状况下33.6 L H2生成液态水时放出的热量是 kJ。
(2)化学反应可视为旧键断裂和新键形成的过程。化学键的键能是形成(或拆开)1mol化学键时释放(或吸收)的能量。已知白磷P4和P4O6的分子结构如下图所示:
现提供以下化学键的键能:P-P 198 kJ·mol-1 P-O 360 kJ·mol-1,氧气分子内氧原子间的(O=O)键能为498 kJ·mol-1。则P4+3O2 = P4O6的反应热ΔH为 。
某科研小组探究工业废Cu粉(杂质含有SiO2、Al2O3、Fe2O3中的一种或几种)的组成并制备少量CuSO4·5H2O,实现废物综合利用,实验过程如下:
过程Ⅰ: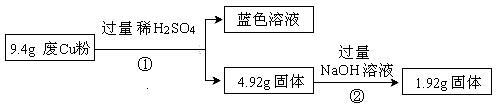
(1)废Cu粉中一定含有的杂质是 (填化学式)。
(2)写出过程②发生反应的离子方程式: 。
过程Ⅱ: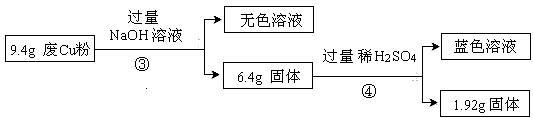
(3)综合过程Ⅰ、II,计算废Cu粉中各成分的质量之比是 (化为最简整数比)
过程Ⅲ:已知25℃时:
| 电解质 |
Cu(OH)2 |
Fe(OH)2 |
Fe(OH)3 |
| 溶度积(Ksp) |
2.2×10-20 |
8.0×10-16 |
4.0×10-38 |
| 开始沉淀时的pH |
5.4 |
6.5 |
3.5 |
| 完全沉淀时的pH |
6.4 |
9.6 |
4.0 |
(4)在Ⅱ中所得蓝色溶液中加入一定量的H2O2溶液,调节溶液的pH范围为 ,然后过滤、结晶,可得CuSO4·5H2O。
(5)下列与 Ⅲ方案 相关的叙述中,正确的是(填字母)。
A.H2O2是绿色氧化剂,在氧化过程中不引进杂质、不产生污染
B.将Fe2+ 氧化为Fe3+ 的主要原因是Fe(OH)2沉淀比Fe(OH)3沉淀较难过滤
C.调节溶液pH选择的试剂可以是氢氧化铜或氧化铜
D.在pH>4的溶液中Fe3+一定不能大量存在
已知SiO2、SO2和CO2都是酸性氧化物,化学性质具有一定的相似性;
Mg和Na的化学性质也具有一定相似性。
I、用如图所示装置进行Mg与SO2反应的实验。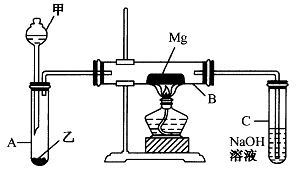
(1)选择制取SO2的合适试剂____________。
①10%的H2SO4溶液②70%的H2SO4溶液③Na2SO3固体 ④CaSO3固体
(2)写出装置B中发生的主要反应的化学方程式___________。
装置C中NaOH溶液的作用是______________。
(3)该装置仍有不足之处,请说明_______________。
Ⅱ、某研究小组进行了“实验室制Si”的研究,它们以课本为基础,查阅资料得到以下可供参考的四条信息:
①Mg在加热的条件下即可与SiO2反应
②金属硅化物与稀H2SO4反应生成硫酸盐与SiH4
③Si和SiO2均不与稀H2SO4反应
④SiH4在空气中自燃
他们在研究报告中记载着“……选用合适的物质在适宜的条件下充分反应;再用足量稀硫酸溶解固体产物;然后过滤、洗涤、干燥;最后称量……在用稀硫酸溶解固体产物时,发现有爆鸣声和火花,其产率也只有预期值的63%左右”。
(4)该小组“实验室制Si”的化学方程式是 。
(5)你估计“用稀硫酸溶解固体产物时,发现有爆鸣声和火花”的原因是(用化学方程式说明): 。
资料表明,硫粉与热的KOH溶液共热生成两种盐,其中一种是K2SO3。某化学兴趣小
组进行该实验时,却检测到生成的盐中含有SO42-。
(1)兴趣小组同学认为,上述反应的生成物可能与反应温度(T),KOH溶液的浓度(c)有关。他们做了如下对比实验(每次实验中硫粉的质量、KOH溶液的体积均相同)。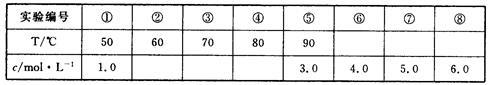
实验①~④是探究温度对生成物的影响,⑤~⑧是探究KOH溶液的浓度对生成物的影响。请在表中相应空格内填人相应数据。
(2)兴趣小组设计实验对上述反应中生成的盐的成分进行探究。他们提出如下假设,请你根据氧化还原反应的规律,完成假设二和假设三:
假设一:生成的盐是K2S和K2 S03;
假设二:生成的盐是____;
假设三:生成的盐是____;
(3)请你设计实验验证上述假设一。完成下表中内容。[除了硫粉与热的KOH溶液的反应液之外,可供选择的药品有稀硝酸,稀盐酸等;已知:6H++SO32-+2S2-=3S+3H2O
(4)兴趣小组通过改变硫粉的质量,得出生成钾盐的质量与硫粉质量的变化关系如图所示。有人据此得出结论:生成的盐一定是K2S和K2SO3的混合物。请你根据计算结果指出该结论是否正确 。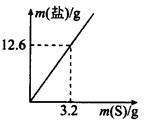
(5)请分析上述反应中有K2S04生成的可能原因是 。
I.高锰酸钾在实验室和工农业生产中有广泛的用途,实验室以二氧化锰为主要原料制
备高锰酸钾,其部分流程如下:
(1)第①步加热熔融应在铁坩埚中进行,而不用瓷坩埚的原因是 (用化学程式表示)。
(2)第④步通人适量CO2,发生反应生成Mn04和Mn02和碳酸盐,则发生反应的离子方程式为___ _。
(3)第⑥步加热浓缩至液面有细小晶体析出时,停止加热,冷却结晶、过滤、洗涤、干燥,干燥过程中,温度不宜过高,其原因是 (用化学方程式表示)。
(4)H2O2和KMn04都是常用的强氧化剂,若向H2O2溶液中滴加酸性高锰酸钾溶液,则酸性高锰酸钾溶液会褪色,写出该反应的离子方程式:_____ 。
Ⅱ.某小组设计如图所示的装置图(图中夹持和加热装置略去),分别研究S02和Cl2的性质。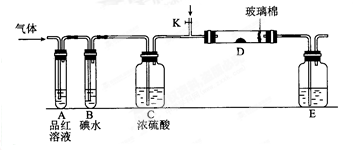
(5)若从左端分别通人SO2和Cl2,装置A中观察到的现象是否相同? (填“相同”或“不相同”);
(6)若装置B中装有5.0 mL l.0 mol/L的碘水,当通入足量Cl2完全反应后,共转移了5.0×10-2 mol电子,该反应的化学方程式为 。
(7)若由元素S和O组成-2价酸根离子X,X中S和O的质量比为4:3;当Cl2与含X的溶液完全反应后,有浅黄色沉淀产生,取上层清液加入氯化钡溶液,有白色沉淀产生。写出Cl2与含X的溶液反应的离子方程式__ __。
硫酸锰可作为饲料添加剂用于增肥,也可用于某些化学反应的催化剂,易溶于水,不溶于乙醇。工业上常用软锰矿(主要成分为MnO2,含有MgSO4等杂质)制备硫酸锰,其简化流程如下: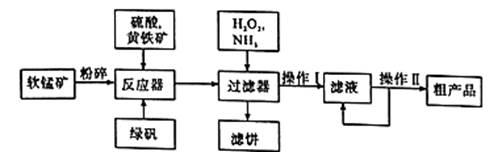
(1)为了加快软锰矿与硫酸、黄铁矿反应的速率,工业上除采用粉碎软锰矿的方法,还可以用哪些方法 (写两种)。
(2)流程中黄铁矿(主要含FeS2)和FeSO4的作用都是作还原剂,请写出FeSO4与软锰矿反应的离子方程式 。
(3)双氧水和氨水的作用分别是 .
(4)操作II包括 、 、 、洗涤、干燥,可制得MnSO4·H2 O粗产品.洗涤中最好选用 ’
| A.稀硫酸 | B.水 | C.乙醇 | D.浓硫酸 |