2SO2(g)+O2(g) 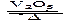 2SO3(g)是制备硫酸的重要反应。下列叙述正确的
2SO3(g)是制备硫酸的重要反应。下列叙述正确的
| A.催化剂V2O5不改变该反应的逆反应速率 |
| B.增大容器体积,反应速率一定增大 |
| C.该反应是放热反应,降低温度将缩短反应达到平衡的时间 |
D.在t1、t2时刻,SO3(g)的浓度分别是c1,c2,则时间间隔t1~t2内,SO3(g)生成的平均速率为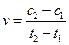 |
下列说法正确的是
| A.金属在反应中只能作还原剂,非金属在反应中只能作氧化剂 |
| B.氧化剂在反应中失去电子,还原剂在反应中得到电子 |
| C.氧化剂具有氧化性,还原剂具有还原性 |
| D.阳离子只有氧化性,阴离子只有还原性 |
丁香油酚的结构简式为 据此结构分析,下列说法正确的是
据此结构分析,下列说法正确的是
| A.可以燃烧,只能与溴水发生加成反应 |
| B.可与NaOH溶液反应,也可与FeCl3溶液反应 |
| C.不能与金属钠反应放出H2 |
| D.可以与小苏打溶液反应放出CO2气体 |
关于海水综合利用问题,下列说法错误的是
| A.从能量转换角度来看,氯碱工业中的电解饱和食盐水是一个将电能转化为化学能的过程 |
| B.在过程②中若要获得无水MgCl2不可直接蒸干灼烧 |
| C.除去粗盐中杂质(Mg2+、SO42﹣、Ca2+),加入的药品顺序为:NaOH溶液→Na2CO3溶液→BaCl2溶液→过滤后加盐酸 |
| D.第③④步的目的是为了浓缩富集溴 |
以下说法错误的是
| A |
2Na+2H2O=2NaOH+H2↑ 2Al+2H2O+2NaOH=2NaAlO2+3H2↑ |
均为水做氧化剂的氧化还原反应 |
| B |
Fe+CuSO4=FeSO4+Cu 2Mg+CO2=2MgO+C |
均为固体质量增大的置换反应 |
| C |
NaAlO2+SO2+2H2O=Al(OH)3+NaHSO3 NaClO+CO2+H2O=HClO+NaHCO3 |
均为较强酸制较弱酸的复分解反应 |
| D |
H2O2+SO2=H2SO4 CaO+SO3=CaSO4 |
均为非氧化还原反应的化合反应 |
A.A B.B C.C D.D
在标准状况下,将wgA气体(摩尔质量为Mg/mol)溶于1L水中,所得溶液密度为dg/mL,则此溶液的物质的量浓度为mol/L.
A. |
B. |
C. |
D. |