已知I- 、Fe2+ 、SO2 、Cl- 和H2O2均有还原性,它们在酸性溶液中还原性的强弱顺序为Cl-<Fe2+<H2O2<I-<SO2,则下列反应中不能发生的是
| A.H2O2 + H2SO4 ══ SO2 ↑ + O2 ↑ + 2H2O |
| B.I2 + SO2 + 2H2O ══ H2SO4 + 2HI |
| C.2Fe2+ + Cl2 ══ 2Fe3+ + 2Cl- |
| D.2Fe3+ + SO2 + 2H2O ══ 2Fe2+ + SO42-+ 4H+ |
下列有关电化学的示意图正确的是( )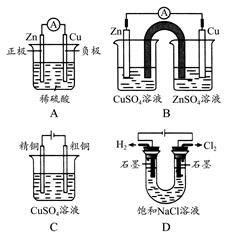
下列过程都与热量变化有关,其中表述不正确的是 ( )
| A.CO(g)的燃烧热是283.0 kJ/mol,则表示CO(g)燃烧反应的热化学方程式为:CO(g)+1/2O2(g)=CO2(g) ΔH=-283.0 kJ/mol |
| B.稀盐酸和稀氢氧化钠溶液反应的中和热为57.3 kJ/mol,则表示稀硫酸与稀氢氧化钡溶液发生反应的热化学方程式为:H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3 kJ/mol |
| C.铝热反应是放热反应,但需要足够的热量才能使反应发生 |
| D.水的电离过程是吸热过程,升高温度,水的离子积增大、pH减小 |
查处酒后驾驶采用的“便携式乙醇测量仪”以燃料电池为工作原理,在酸性环境中,理论上乙醇可以被完全氧化为CO2,但实际乙醇被氧化为X,其中一个电极的反应式为CH3CH2OH-2e-=X+2H+。下列说法中正确的是 ( )
| A.电池内部H+由正极向负极移动 |
| B.另一极的电极反应式为:O2+4e-+2H2O=4OH- |
| C.乙醇在正极发生反应,电子经过外电路流向负极 |
| D.电池总反应为:2CH3CH2OH+O2=2CH3CHO+2H2O |
下列说法不正确的是 ( )
| A.粗铜电解精炼时,应将粗铜与直流电源的正极相连 |
| B.金属的吸氧腐蚀的过程中,正极的电极反应式为O2+2H2O+4e-=4OH- |
| C.燃料电池中加入燃料的电极一定是电池的负极 |
| D.在生产生活中,为保护钢铁器件免受腐蚀,应将该器件与直流电源的正极相连 |
①②③④四种金属片两两相连浸入稀硫酸中都可组成原电池。①②相连时,外电路电流从②流向①:①③相连时,③为正极:②④相连时,②上有气泡逸出:③④相连时,③的质量减少,据此判断这四种金属活动性由大到小的顺序是 ( )
| A.①③②④ | B.①③④② | C.③④②① | D.③①②④ |