相同温度下,体积均为0.25L的两个恒容密闭容器中发生可逆反应:
X2(g)+3Y2(g) 2XY3(g) △H=-92.6kJ·mol-1
2XY3(g) △H=-92.6kJ·mol-1
起始时各物质物质的量如下表所示:
| 容器 编号 |
起始时各物质物质的量/mol |
||
| X2 |
Y2 |
XY3 |
|
| ① |
1 |
3 |
0 |
| ② |
0.6 |
1.8 |
0.8 |
达到平衡后,①容器中XY3的物质的量为0.5mol。下列叙述正确的是
A.容器①、②中反应的平衡常数不相等
B.达平衡时,容器②中XY3的物质的量浓度为2mol·L—1
C.容器①中反应达到平衡时放出的热量为23.15 kJ
D.容器②中反应达到平衡时放出热量
对于下列事实的解释错误的是()
①蔗糖中加入浓H2SO4后出现发黑现象,说明浓硫酸具有脱水性②浓硝酸的颜色变黄,说明浓硝酸见光易分解③SO2气体通入溴水使溴水褪色,说明SO2具有漂白性④常温下浓硫酸可用铁槽车储运,说明常温下浓硫酸跟铁不反应
| A.①②③④ | B.③④ | C.只有③ | D.只有④ |
下列除杂质的方法正确的是()
| A.用过量的碱液除去CO2中混有的少量HCl气体 |
| B.用饱和食盐水除去氯气中混有的SO2气体 |
| C.用升华的方法除去食盐中少量的I2 |
| D.用过量的氯化钡溶液除去亚硫酸钠溶液中的少量SO42- |
目前,我国城市环境污染中的大气污染物主要是()
| A.NH3、NO、CO2、雾 | B.CO2、N2、Cl2、酸雨 |
| C.SO2、NO2、CO、烟尘 | D.HCl、SO2、N2、沙尘暴 |
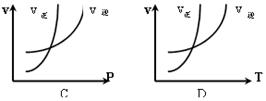
对于反应:N2+3H2 2NH3(正反应为放热反应),下列图象所示不正确的是()
2NH3(正反应为放热反应),下列图象所示不正确的是()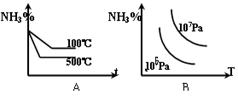
w
人体血液内的血红蛋白(Hb)易与O2结合生成HbO2,因此具有输氧能力CO吸入肺中发生反应:CO+HbO2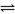 O2+HbCO ,37 ℃时,该反应的平衡常数K="220" 。HbCO的浓度达到HbO2浓度的0.02倍,会使人智力受损。据此,下列结论错误的是 ( )
O2+HbCO ,37 ℃时,该反应的平衡常数K="220" 。HbCO的浓度达到HbO2浓度的0.02倍,会使人智力受损。据此,下列结论错误的是 ( )
A.CO与HbO2反应的平衡常数K= |
| B.人体吸入的CO越多,与血红蛋白结合的O2越少 |
| C.当吸入的CO与O2浓度之比大于或等于0.02时,人的智力才会受损 |
| D.把CO中毒的病人放入高压氧仓中解毒,其原理是使上述平衡向左移动 |