用CH4催化还原NOx可以消除氮氧化物的污染。例如
①CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g);ΔH=-574kJ/mol
②CH4(g)+4NO(g) =2N2(g)+CO2(g)+2H2O(g);ΔH=-1160kJ/mol 下列说法不正确的是
| A.由反应①可推知:CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(l);ΔH=-Q kJ/mol,Q>574 |
B.等物质的量的甲烷分别参加反应①、②,反应转移的电子数不同 |
C.若用标准状况下4.48LCH4还原NO2至N2,放出的热量为173.4kJ |
D.若用标准状况下4.48LCH4还原NO2至N2,整个过程中转移的电子总数为1.6mol |
下列有关气体体积的叙述,正确的是()
| A.一定温度、压强下,气态物质体积的大小由构成气体的分子大小决定 |
| B.一定温度、压强下,气态物质体积的大小由构成气体的分子数决定 |
| C.不同的气体,若体积不同,则它们所含的分子数也不同 |
| D.气体摩尔体积是指1 mol任何气体所占的体积约为22.4 L |
在同温、同压下1 mol Ar和1 mol F2,具有相同的()
| A.质子数 | B.质量 | C.原子数 | D.体积 |
下列说法不正确的是()
| A.磷酸的摩尔质量与6.02×1023个磷酸分子的质量在数值上相等 |
| B.6.02×1023个氮分子和6.02×1023个氢分子的质量比等于14∶1 |
| C.32 g 氧气所含的原子数目为2×6.02×1023 |
| D.常温、常压下,0.5×6.02×1023个一氧化碳分子所占体积是11.2 L |
如下图所示横坐标表示完全燃烧时耗用可燃气体X(X=A、B、C)的物质的量n(X),纵坐标表示消耗O2的物质的量n(O2),A、B是两种可燃气体,C是A和B的混合气体,则C中n(A)∶n(B)为()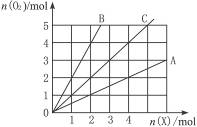
A.2∶1 B.1∶2 C.1∶1 D.任意比
在两个容积相同的容器中,一个盛有HCl气体,另一个盛有H2和Cl2的混合气体。在同温、同压下,两容器内的气体一定具有相同的()
| A.原子数 | B.密度 | C.质量 | D.质子数 |