分类是学习和研究化学的一种常用的科学方法。下列分类合理的是
①根据反应中是否有电子的转移将化学反应分为氧化还原反应和非氧化还原反应
②根据电解质在熔融状态下能否完全电离将电解质分为强电解质和弱电解质
③根据元素原子最外层电子数的多少将元素分为金属和非金属
④根据反应的热效应将化学反应分为放热反应和吸热反应
| A.②③ | B.②③④ | C.①② | D.①④ |
下列离子方程式书写不正确的是
A.往NaOH溶液中通入过量CO2 |
B.单质硅与烧碱溶液反应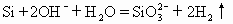 |
C.石英砂与烧碱反应制水玻璃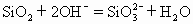 |
| D.往水玻璃中通入二氧化碳 |
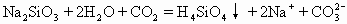
将过量的CO2通入下列溶液中,最终出现浑浊的是
| A.CaCl2溶液 | B.石灰水 |
| C.饱和Na2CO3溶液 | D.水玻璃 |
下列说法正确的是
| A.二氧化硅溶于水显酸性 |
| B.光导纤维传导光的能力非常强,利用光缆通讯,能同时传送大量信息 |
| C.因为高温时二氧化硅与碳酸钠反应放出CO2,所以硅酸的酸性比碳酸强 |
| D.二氧化硅是酸性氧化物,它不溶于任何酸。 |
下列溶液中可以盛放在玻璃瓶中,但不能用磨口玻璃塞的是
|
熔融氢氧化钠反应选用的器皿是
|