①A、B、C、D、E是周期表中短周期元素,它们的原子序数依次增大,A和D的最外层电子数是其电子层数的2倍,B和D同主族,C的原子是短周期元素中原子半径最大的。请回答:
(1)写出元素名称:A 、B 。
(2)已知AD2与AB2的结构相似,AD2的结构式为 ,
该分子是 (填“极性”或“非极性”)分子。
(3)常温下将E单质通入到C的最高价氧化物对应的水化物溶液里发生反应的离子方程
式为 。
(4)请写出B和C按原子个数比1∶1形成的化合物与A和B按按原子个数比1∶2形成的化合物反应的化学方程式,并标出电子转移的方向和数目 。
②下表是元素周期表的一部分。表中所列的字母分别代表某一种化学元素。
| Z |
|
|
|
|
|||||||||||||
| |
|
M |
L |
Q |
R |
|
|
||||||||||
| D |
A |
|
|
T |
X |
Y |
|
||||||||||
| E |
|
|
|
|
|
|
|
|
J |
|
|
|
|
|
|
|
|
(1)Y分别与D、E形成的化合物中熔点较高是_________(用具体物质的化学式表示)。
(2)LY4分子的电子式是_____ ____。
(3)由J、L、R三种元素形成的某种配位化合物,常温下该化合物具有挥发性,化学式为J(LR)4,其中J的化合价是0价。J(LR)4固态时属于_________晶体(填晶体类型)。
(4)A与M组成的一种化合物AM2,刷新了金属化合物超导温度
的最高记录。下图中所示的是该化合物的晶体结构单元。图中
上、下底面中心“Δ”处的原子是_______(填元素符号)。
某研究性学习小组在实验室合成了一种物质A。
(1)已知:A的相对分子质量不超过100,4.3g A在氧气中完全燃烧,生成的气体通过浓硫酸,浓硫酸增重4.5g;剩余气体通过碱石灰,碱石灰增重11.0g则A的分子式为
(2)该兴趣小组同学对物质A结构进行了预测,其中不正确的是(填序号)
A.可能含有一个碳环和一个醛基
B.可能含有一个碳碳双键和一个羟基
C.可能只含一个碳氧双键官能团
D.可能是环状的醚
(3)若A的核磁共振氢谱如下图所示,且A可以和金属钠反应生成H2,但不能在Cu作催化剂下被催化氧化。(提示:羟基与碳碳双键相连的结构不稳定)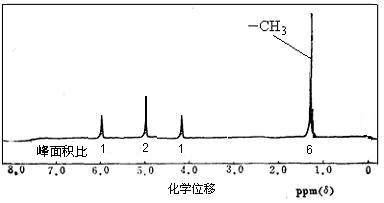
请根据以上信息写出A的结构简式。
(4)已知 “C=C=C”的结构是不稳定的,A 在一定条件下发生消去反应可以生成天然橡胶的单体,写出该反应的化学方程式(并注明条件)
在一定条件下发生消去反应可以生成天然橡胶的单体,写出该反应的化学方程式(并注明条件)
。
塑料是日常生活中常用的高分子合成材料,常用塑料F、G均可由某烃经下列反应得到: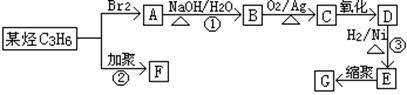
(1)写出反应①、③的反应类型:、。
(2)写出C3H6的同分异构体的结构简式:;B和D都易溶于水,提供一种试
剂加以鉴别,试剂名称为。
(3)写出反应②的化学方程式:。
(4)写出用新制氢氧化铜悬浊液完成C→D反应的化学方程式:。
(5)写出高分子化合物G的结构简式
(5分) 常温下,有浓度均为0.5mol/L的四种溶液:①Na2CO3②NaHCO3③HCl ④NH3・H2O
(1)上述溶液中,可发生水解的是(填序号)。
(2)向溶液④中加入少量氯化铵固体,此时c(NH4+)/c(OH-)的值(填增大、减小或不变)。
(3)若将③和④的溶液混合后溶液恰好呈中性,则混合前③的体积④的体积(填“>”、“=”或“<”),此时溶液中离子浓度由大到小的顺序是。
(4)取10mL溶液③,加水稀释到500mL,则该溶液中由水电离出的c(H+ )=。
)=。
(7分)
(Ⅰ)CuCl2溶液有时呈黄色,有时呈绿色或蓝色,这是因为CuCl2溶液中存在平衡:
[Cu(H2O)2]2++4Cl- [CuCl4]2-+4H2O。试回答下列问题:
[CuCl4]2-+4H2O。试回答下列问题:
(蓝色)(黄色)
(1)欲使溶液由蓝色变为黄色,可采取的措施是。
(2)欲使溶液由黄色变为蓝色(或黄绿色),可采取的措施是或。
(Ⅱ)有下列5种有机化合物,请按要求填空:
(1)属于酯类的是(填编号,下同);可归类于酚类的是。
(2)既能与NaOH溶液反应,又能与HCl溶液反应的是。
(3)用系统命名法给B物质命名。
一氧化碳与水蒸气的反应为CO(g) + H2O(g)  CO2(g) + H2(g)在密闭容器中,将1.0 mol CO与1.0mol H2O混合加热到434℃,在434℃的平衡常数K1 =9
CO2(g) + H2(g)在密闭容器中,将1.0 mol CO与1.0mol H2O混合加热到434℃,在434℃的平衡常数K1 =9
(1)跟踪测定H2O的物质的量浓度,如图所示,则0 —20 min ,H2O的反应速率是
(2)请在图中用实线绘制出在该温度下加入正催化剂后,H2O的物质的量浓度变化图线。
(3)从434℃升温至800℃,800℃的平衡常数K2 =1,则正反应为_____________(填“放
热反应”或“吸热反应”或“不能确定”)。
(4)求在800℃反应达平衡时,CO转化为CO2的转化率(写出必要的计算过程)