下图是用0.1000 mol/L的盐酸滴定某未知浓度的 NaOH溶液的示意图和某次滴定前、后的盛放盐酸滴定管中液面的位置。请回答:
NaOH溶液的示意图和某次滴定前、后的盛放盐酸滴定管中液面的位置。请回答:
⑴ 仪器A的名称是 ;
⑵ 盐酸的体积读数:滴定前读数为 mL,滴定后读数为 mL 。
⑶ 某实验小组同学的三次实验的实验数据如下表所示。 根据表中数据计算出的待测NaOH溶液的平均浓度是 mol/L。(保留四位有效数字)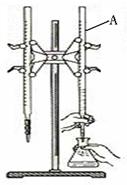

| 实验 编号 |
待测NaOH溶液的体积(mL) |
滴定前盐酸的 体积读数(mL) |
滴定后盐酸的 体积读数(mL) |
| 1 |
20.00 |
1.20 |
23.22 |
| 2 |
20.00 |
2.21 |
24.21 |
| 3 |
20.00 |
1.50 |
23.48 |
⑷ 滴定操作可分解为如下几步(所用的仪器刚用蒸馏水洗净):
| A.用碱式滴定管向锥形瓶里注入20.00 mL待测NaOH溶液,并加入2~3滴酚酞; |
| B.用标准溶液润洗酸式滴定管2~3次; |
| C.把盛有标准溶液的酸式滴定管固定好,调节滴定管尖嘴使之充满溶液,使管内无气泡; |
| D.取标准HCl溶液注入酸式滴定管至刻度0以上2~3 cm; |
E.调节液面至0或0以下刻度,记下读数;
F.把锥形瓶放在滴定管的下面,用标准HCl溶液滴定至终点并记下滴定管液面的刻度。
正确操作步骤的顺序是(用序号字母填写)________
⑸用标准盐酸滴定待测烧碱溶液,滴定时____手旋转酸式滴定管的 ,_______手不停地向同一方向摇动锥形瓶,两眼注视 ,直到 为止,可判断滴定到达终点。
实验室有下列仪器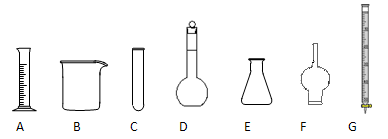
请从A~G中选择适当的装置填空(填字母),并指出其名称。
(1)蒸馏实验中要用到的是,它的名称为______。
(2)配制一定物质的量浓度的溶液要用到、需要垫上石棉网才可以加热的是,它的名称为______。
(3)常盛放固体干燥剂,用以干燥气体的是______,它的名称为______。
碱式碳酸镁密度小,是橡胶制品的优良填料。可用复盐MgCO3·(NH4)2CO3·H2O作原料制备。取一定量的含镁复盐放入三颈烧瓶中,并将三颈烧瓶放在恒温水浴锅中加热(如图所示),按一定的液固比加入蒸馏水,开启搅拌器同时加入预定的氨水,待温度到达 40℃时开始热解,此时滴加卤水(氯化镁溶液)并继续滴入氨水,保持10分钟,一段时间后过滤洗涤,滤出的固体在 120℃干燥得到碱式碳酸镁产品。
(1)①搅拌的目的是 ,②选择水浴加热方式,其优点是: 。
(2) 40℃复盐开始热解生成MgCO3·3H2O,该反应的化学方程式为: 。
(3)40℃时,开始滴加卤水的目的是
(4)碱式碳酸镁产品中镁的质量分数(ω(Mg)%)越高,产品质量越好,氯的质量分数越高,产品质量越差。分析Cl-含量采用滴定法,先精确称取一定量产品用适量硝酸溶解,经稀释等步骤最终配得一定体积的溶液。
测定实验中除用到天平、烧杯、玻璃棒、锥形瓶、滴定管外,还用到的玻璃仪器有: 。
(5)若已知制得的碱式碳酸镁的质量ag,要确定其组成(不考虑微量杂质),还必需的数据有: 。
①充分灼烧后,剩余固体的质量 ②灼烧时,测算得的二氧化碳的体积(已换算成标准状况)③灼烧时的温度和时间 ④碱式碳酸镁的密度
无水亚硫酸钠隔绝空气加热到600℃便开始分解,分解产物是硫化钠和另外一种固体。某学生将无水亚硫酸钠受热后的试样溶于水制成浓溶液,用下图所示的实验装置进行实验,他向试样溶液中缓缓地逐滴加入稀盐酸,根据实验现象判断固体试样含有什么成分?
(1)如果加热温度在600℃以上,再向所得固体的试样溶液中缓缓滴加稀盐酸至足量,观察到品红溶液不褪色,CuSO4溶液中出现黑色沉淀,试分析试样溶液中可能出现的现象___________________,解释这种现象的离子方程式是_______________;品红溶液不褪色的原因是:_____________________。
(2)通过上述实验现象推断无水亚硫酸钠受热分解的化学方程式是____________________,装置中的NaOH溶液的作用是____________________________。
(3)若加入了足量的稀盐酸后,品红溶液和CuSO4溶液中都无明显的现象发生,原因是_____________________________________。
为了探究HClO的漂白性,某同学设计了如下的实验。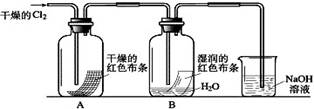
(1)通入Cl2后,从集气瓶A中干燥的红色布条的现象可得出的结论是;从集气瓶B中湿润的红色布条的现象可得出的结论是,其中发生的反应的化学方程式为。
(2)为了确证是HClO使湿润的红色布条褪色,你认为还应增加的实验是。
(3)烧杯中溶液所起的作用是,烧杯中所发生反应的化学方程式为。
(4)为保证实验安全,当氯气以每分钟1.12L(标准状况)的流速匀速通入时,若实验需耗时4分钟,小烧杯中盛2 mol·L—1的NaOH溶液的体积至少应为__________mL。
实验室欲配制250mL 0.2 mol·L-1的碳酸钠溶液,回答下列问题:
可供选择的仪器:①量筒②胶头滴管③托盘天平④药匙⑤烧瓶⑥烧杯
(1)通过计算可知,应用托盘天平称取g碳酸钠晶体(Na2CO3•10H2O)。
(2)配制过程需要的仪器______________(填序号),还缺少的仪器有。
(3)配制时,正确的操作顺序是(用字母表示,每个字母只能用一次)_____________;
| A.用30mL水洗涤烧杯2~3次,洗涤液均注入容量瓶 |
| B.用托盘天平准确称取所需的Na2CO3固体的质量,放入烧杯中,再加入少量水(约30mL),用玻璃棒慢慢搅动,使其充分溶解 |
| C.将已冷却的溶液沿玻璃棒注入250mL的容量瓶中 |
| D.将容量瓶盖紧,振荡,摇匀 |
E.改用胶头滴管加水,使溶液凹面恰好与刻度相切
F.继续往容量瓶内小心加水,直到液面接近刻度1~2cm处
(4)若出现如下情况,对所配溶液浓度将有何影响(填“偏高”、“偏低”或“无影响”)。若没有进行A操作______________;若定容时俯视刻度线_______________。