下图是三种稀酸对Fe – Cr合金随Cr含量变化的腐蚀性实验结果,下列有关说法正确的是:
| A.稀硫酸对Fe – Cr合金的腐蚀性比稀硝酸和稀盐酸的强 |
| B.稀硝酸和铁反应的化学方程式是: Fe + 6HNO3(稀) = Fe(NO3)3 + 3NO2↑+3H2O |
| C.随着Cr含量的增加,稀硝酸对Fe – Cr合金的腐蚀性减弱 |
D.Cr含量大于13%时,因为三种酸中 硫酸的氢离子浓度最大,所以对Fe – Cr合金的腐蚀性最强 硫酸的氢离子浓度最大,所以对Fe – Cr合金的腐蚀性最强 |
CO2与H2的混合气体5g,在150℃时和足量的氧气混合,用电火花充分引燃,在相同状况下再将反应后所得混合气体通入到足量的Na2O2中,测得Na2O2固体增重的质量为3.4g,则原混合气体中CO2的物质的量分数为
| A.25% | B.75% | C.88% | D.32% |
已知次氯酸是比碳酸还弱的酸,反应Cl2+H2O  H+ +Cl- + HClO达到平衡后,要HClO浓度增大,可加入()
H+ +Cl- + HClO达到平衡后,要HClO浓度增大,可加入()
| A.Na 2SO3固体 | B.水 | C.CaCO3固体 | D.NaOH固体 |
已知下列数据
| 化学键 |
H—H |
Cl—Cl |
H—Cl |
| 生成(拆开)1mol化学键放出(吸收)的能量 |
436kJ |
243kJ |
431kJ |
则下列热化学方程式不正确的是
A、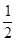 H2(g)+
H2(g)+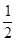 Cl2(g)="=HCl(g)" ;△H=-91.5kJ·mol-1
Cl2(g)="=HCl(g)" ;△H=-91.5kJ·mol-1
B、H2(g)+ Cl2(g)="=2HCl(g)" ;△H=-183kJ·mol-1
C、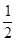 H2(g)+
H2(g)+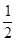 Cl2(g)="=HCl(g)" ;△H=+91.5kJ·mol-1
Cl2(g)="=HCl(g)" ;△H=+91.5kJ·mol-1
D、2HCl(g) ==H2(g)+ Cl2(g) ;△H=+183kJ·mol-1
近年来,科学家研制了一种新型的乙醇电池,它用酸性电解质(H+)作溶剂。电池总反应为:C2H5OH+3O2=2CO2+3H2O,下列说法不正确的是
| A.乙醇在电池的负极上参加反应 |
| B.1mol CH3CH2OH被氧化转移6mol e- |
| C.随着反应的进行,正极附近的酸性减弱。 |
| D.电池正极的正极反应为4H++O2+4e-=2H2O |
碱性电池具有容量大、放电电流大的特点,因而得到广泛应用。锌—锰碱性电池以氢氧化钾溶液为电解液,电池总反应式为:Zn(s)+2MnO2(s)+H2O(l)==Zn(OH)2(s)+Mn2O3(s)
下列说法错误的是()
| A.电池工作时,锌失去电子 |
| B.电池工作时,电子由正极通过外电路流向负极 |
| C.电池正极的电极反应式为:2MnO2(s)+H2O(1)+2e—=Mn2O3(s)+2OH—(aq) |
| D.外电路中每通过O.2mol e-,锌的质量理论上减小6.5g |