用NA表示阿伏加德罗常数的值。下列叙述正确的是
| A.标准状况下,11.2 L水中含有的分子数是0.5NA |
| B.常温常压下,17g氨气中所含原子数为NA |
| C.23g钠与一定量的氧气作用,若两者均无剩余,转移NA个电子 |
| D.100mL 3 mol•L-1盐酸与5.6g Fe充分反应转移0.3 NA个电子 |
向某恒容密闭容器中充入一定量C02和H2,发生反应: 测得平衡体系中C02的百分含量(C02%)与反应温度变化的关系如图所示。下列物理量中,a点大于b点的是
测得平衡体系中C02的百分含量(C02%)与反应温度变化的关系如图所示。下列物理量中,a点大于b点的是
①:正反应速率 ②逆反应速率 ③HCOOH(g)的浓度 ④对应温度时的平衡常数
| A.①② | B.①③ | C.②④ | D.③④ |
用CO合成甲醇(CH3OH)的化学方程式为CO(g)+2H2(g)⇌CH3OH(g)△H<0,按照相同的物质的量投料,测得CO在不同温度下的平衡转化率与压强的关系如图所示.下列说法正确的是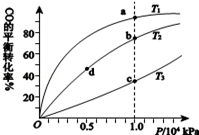
| A.温度: T1>T2>T3 |
| B.正反应速率:υ(b)>υ(d) υ(a)>υ(c) |
| C.平衡常数:K(a)>K(c) K(b)=K(d) |
| D.平均摩尔质量: M(b)>M(d) M(a)<M(c) |
下列说法不正确的是
| A.一定温度下,在固定体积的密闭容器中发生可逆反应A(s)+B(g)═C(g)+D(g),当混合气体的密度不再改变时,说明已达到化学平衡状态 |
| B.对于反应C(s)+CO2(g)═2CO(g)△H>0,改变某一条件,若化学平衡常数增大,则反应速率也一定增大 |
C.常温下向0.1mol•L﹣1的NH3•H2O中加入氯化铵固体,则溶液中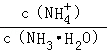 减小 减小 |
D.常温下向Mg(OH)2悬浊液中加入MgCl2浓溶液,溶液中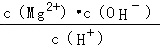 不变 不变 |
下列说法不正确的是
①将CO2通入BaCl2溶液中,始终无白色沉淀生成
②将盐酸、KSCN溶液和Fe(NO3)2溶液三种溶液混合,混合溶液显红色
③向某溶液中滴入盐酸酸化的BaCl2溶液产生白色沉淀,证明溶液中一定含有SO42﹣
④将两小块质量相等的金属钠,一块直接投入水中,另一块用铝箔包住,在铝箔上刺些小孔,然后投入水中,两者放出的氢气质量相等
⑤将SO2通入溴水中,证明SO2具有漂白性
⑥滴有酚酞的Na2CO3溶液中,加BaC12溶液红色逐渐褪去,证明Na2CO3溶液中存在水解平衡
⑦因为SiO2能和CaCO3反应生成CO2,所以H2SiO3酸性强于H2CO3.
| A.②④⑥⑦ | B.①③④⑤ | C.③④⑤⑦ | D.②③④⑤⑦ |
NO2、O2和熔融KNO3可制作燃料电池,其原理如图,该电池在使用过程中石墨I电极上生成氧化物Y,Y可循环使用。下列说法正确的是
| A.O2在石墨Ⅱ附近发生氧化反应 |
| B.该电池放电时NO3-向石墨Ⅱ电极迁移 |
C.石墨Ⅰ附近发生的反应:3NO2 +2e- NO+ 2NO3- NO+ 2NO3- |
| D.相同条件下,放电过程中消耗的NO2和O2的体积比为4∶1 |