用CO合成甲醇(CH3OH)的化学方程式为CO(g)+2H2(g)⇌CH3OH(g)△H<0,按照相同的物质的量投料,测得CO在不同温度下的平衡转化率与压强的关系如图所示.下列说法正确的是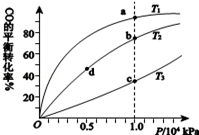
| A.温度: T1>T2>T3 |
| B.正反应速率:υ(b)>υ(d) υ(a)>υ(c) |
| C.平衡常数:K(a)>K(c) K(b)=K(d) |
| D.平均摩尔质量: M(b)>M(d) M(a)<M(c) |
对于达到平衡的反应:2A(g)+B(g)  nC(g),符合右图所示的结论是
nC(g),符合右图所示的结论是
| A.P1>P2,n>3 | B.P1>P2,n<3 |
| C.P1<P2, n>3 | D.P1<P2, n<3 |
下列电离方程式书写正确的是
A.H2S 2H++S2- 2H++S2- |
B.Al(OH)3==Al3+ + 3OH- |
C.NH3·H2O NH4+ +OH- NH4+ +OH- |
D.NaHCO3 ==Na++ H+ + CO32- |
汽车尾气的无害化处理的反应为2CO(g)+2NO(g) N2(g)+2CO2(g) △H<0下列说法不正确的是
N2(g)+2CO2(g) △H<0下列说法不正确的是
| A.升高温度,正逆反应速率都加快 | B.使用催化剂,正逆反应速率都加快 |
| C.使用催化剂,可以降低活化能 | D.升高温度,上述反应的平衡常数会增大 |
体积相同的甲、乙两个容器中,分别都充有等物质的量的SO2和O2,在相同温度下发生反应:2SO2(g)+ O2(g)===2SO3(g)并达到平衡,反应过程中,甲容器保持体积不变,乙容器保持压强不变,若甲容器中SO2的转化率为P%,则乙容器中SO2的转化率为
| A.等于P% | B.大于P% | C.小于P% | D.无法判断 |
下列物质中, 导电性能最差的是
导电性能最差的是
| A.熔融氢氧化钠 | B.石墨棒 |
| C.盐酸溶液 | D.固体氯化钠 |