下列有关实验的叙述中,正确的是 ( )
①用湿润的pH试纸测定溶液的pH
②不宜用瓷坩埚熔融氢氧化钠固体或碳酸钠固体
③可用加热法分离I2和NH4Cl的混合物
④可用稀硝酸洗涤“银镜反应”实验后附着在试管壁上的银
⑤向沸腾的NaOH稀溶液中滴加FeCl3饱和溶液,可以制得Fe(OH)3胶体
⑥实验室配制氯化亚铁溶液时,可先将氯化亚铁溶解在盐酸中,再加入蒸馏水稀释,最后加入少量铁粉
| A.①②④ | B.②③⑥ | C.②④⑥ | D.②③④⑤⑥ |
下列说法正确的是()
| A.pH=2与pH=1的硝酸中c(H+)之比为1:10 |
| B.Na2CO3溶液中c(Na+)与c(CO32-)之比为2:1 |
| C.0.2 mol•L-1与0.1mol/L醋酸中c (H+)之比为2:1 |
| D.NO2溶于水时,被氧化的n(NO2)与被还原的n(NO2)之比为3:1 |
1体积pH=2.5的盐酸与10体积某一元强碱溶液恰好完全反应,则该碱溶液的pH等于
| A.9.0 | B.9.5 | C.10.5 | D.11.5 |
下列操作中能使电离平衡H2O H++OH-,向右移动且溶液呈酸性的是()
H++OH-,向右移动且溶液呈酸性的是()
| A.向水中加入NaHSO4溶液 | B.向水中加入Al2(SO4)3固体 |
| C.向水中加入Na2CO3溶液 | D.将水加热到100℃,使pH=6 |
在一密闭容器中进行反应 X2(g)+ 3Y2(g)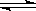 2Z2(g),若 X2、Y2、Z2的起始浓度分别为0.1mol/L、0.3 mol/L、0.2 mol/L,当反应达到平衡后,各物质的浓度有可能是()
2Z2(g),若 X2、Y2、Z2的起始浓度分别为0.1mol/L、0.3 mol/L、0.2 mol/L,当反应达到平衡后,各物质的浓度有可能是()
| A.c(X2)=0.2 mol/L | B.c(Y2)=0.1 mol/L |
| C.c(Z2)=0.4 mol/L | D.c(Y2)=0.6 mol/L |
对已达化学平衡的下列反应:2X(g)+Y(g) 2Z(g) 其它条件不变,减小压强时,对反应产生的影响是( )
2Z(g) 其它条件不变,减小压强时,对反应产生的影响是( )
| A.逆反应速率增大,正反应速率减小,平衡向逆反应方向移动 |
| B.逆反应速率减小,正反应速率增大,平衡向正反应方向移动 |
| C.正、逆反应速率都减小,平衡向正反应方向移动 |
| D.正、逆反应速率都减小,平衡向逆反应方向移动 |