某钠盐溶液中可能含有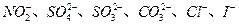 等阴离子。某同学取5份此溶液样品,分别进行了如下实验:
等阴离子。某同学取5份此溶液样品,分别进行了如下实验:
①用pH计测得溶液pH大于7
②加入盐酸,产生有色刺激性气体
③加入硝酸酸化的AgNO3溶液产生白色沉淀,且放出有色刺激性气体
④加足量BaCl2溶液,产生白色沉淀,该沉淀溶于稀硝酸且放出气体,将气体通入品红溶液,溶液不褪色。
⑤加足量BaCl2溶液,产生白色沉淀,在滤液中加入酸化的(NH4)2Fe(SO4)溶液,再滴加KSCN溶液,显红色
该同学最终确定在上述六种离子中只含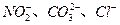 三种阴离子。
三种阴离子。
请分析,该同学只需要完成上述哪几个实验,即可得出此结论。
| A.①②④⑤ | B.③④ | C.③④⑤ | D.②③⑤ |
下列烃中经催化加氢,不能得到2-甲基丁烷的是
| A.2-甲基-1-丁烯 | B.2-甲基-2-丁烯 |
| C.3-甲基-1-丁炔 | D.3,3-二甲基-1-丁炔 |
用下图所示装置及药品进行相应实验,能达到实验目的的是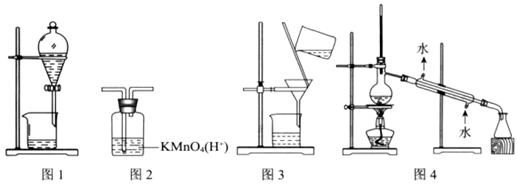
| A.图1分离乙醇和乙酸 | B.图2除去乙炔中的乙烯 |
| C.图3除去溴苯中的溴单质 | D.图4除去工业酒精中的甲醇 |
下列化学方程式不正确的是
A.乙醇与浓氢溴酸反应 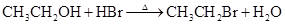 |
B.溴乙烷与氢氧化钠溶液共热 |
C.苯酚钠中通入二氧化碳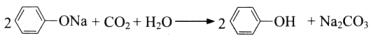 |
D.蔗糖在稀硫酸作用下水解 |
下列醇类物质中,能被氧化成醛的是
下列实验操作不正确的是
| A.实验室制乙烯时,为防止暴沸,应加入沸石 |
| B.不慎将苯酚溶液沾到皮肤上,应立即用稀NaOH溶液清洗 |
| C.饱和食盐水替代水跟电石作用,可以有效控制产生乙炔的速率 |
| D.向AgNO3溶液中逐滴加入稀氨水,至沉淀恰好溶解,制得银氨溶液 |