如图所示,在一烧杯中盛有H2SO4溶液,同时有一表面光滑的塑料小球悬浮于溶液中央,向该烧杯中缓缓注入 Ba(OH)2溶液至恰好完全反应[设H2SO4和Ba(OH)2溶液密度相同]。试回答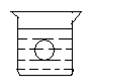
⑴此实验中,观察到的现象有:
① , ② 。
⑵写出实验过程中反应的离子方程式为 。
某校化学研究性学习小组利用下面所提供的仪器装置和药品制取NaHCO3溶液,设计如下实验。实验室提供的药品、仪器装置如下:
药品:①2% NaOH溶液 ②稀HCl ③稀H2SO4 ④饱和KHCO3溶液 ⑤浓H2SO4 ⑥CaCO3固体 ⑦K2CO3粉末
仪器装置(如图所示):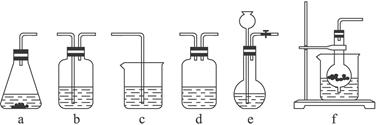
请根据题目要求完成下列问题:
(1)请按下表要求,填写选择的装置和药品。
| 分项 内容 |
CO2发生装置(随开随用,随关随停)(X) |
除杂洗气装置(Y) |
制备产品装置(Z) |
| 选择的装置(填序号) |
c |
||
| 选择的药品(填序号) |
① |
(2)如何检验所选择的CO2发生装置(X)的气密性,请写出主要操作过程:_________________。
(3)将装置按X、Y、Z顺序连接并检查气密性后,当加入药品实验时,X装置中发生化学反应的离子方程式为________________________,Y装置中除去的杂质为_____________。
(4)常温下,向Z装置的NaOH溶液中通入过量CO2气体,其目的是____________________。
(5)若要保证Z装置中不析出晶体(不考虑过饱和溶液问题),NaOH溶液最大浓度不能超过_______________%(质量分数)。
附:有关物质在常温(25 ℃)时的溶解度
| 化学式 |
Na2CO3 |
NaHCO3 |
NaOH |
NaCl |
Na2SO4 |
| 溶解度(g/100 g H2O) |
21.3 |
9.60 |
107 |
35.8 |
19.4 |
【提出猜想】
Ⅰ.所得溶液中的金属离子可能含有Fe2+和Fe3+中的一种或两种;
Ⅱ.所得气体中可能含有 ▲ 中的一种或两种。
【实验探究】
| 实验操作 |
预期现象 |
结论 |
|
| 验证猜想Ⅰ |
步骤①:取少量0.01 mol/L 酸性KMnO4溶液,滴入所得溶液 |
▲ |
▲ |
| 步骤②: ▲ |
▲ |
含有Fe3+ |
|
| 验证猜想Ⅱ |
将所得气体通入如下装置 |
▲ |
含有两种气体 |
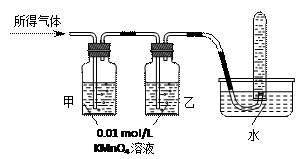
【问题讨论】
有同学提出,若另外选用KSCN溶液,则仅利用KSCN和H2O2两种溶液即可完成猜想Ⅰ的所有探究,请对该观点进行评价: ▲ 。
(福建师大附中2008-2009学年高三第一学期第一学段检测,化学,22)(1)用5.0mol/L的NaOH溶液配制2.0mol/L的NaOH溶液时,下图所示的仪器中,肯定不需要的是 (填序号),配制上述溶液还需要的玻璃仪器是 (填仪器名称)。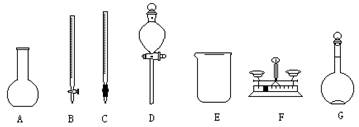
(2)在配制过程中,下列操作将导致实际所配NaOH溶液浓度偏低的是(填编号) _ _。
①准确取出的浓NaOH溶液在空气中露置时间过长;②用量器将浓NaOH溶液直接加入容量瓶,缓慢加入蒸馏水至液面最低点恰好和环形刻度线相切;③摇匀后,液面低于刻度线,再加蒸馏水至液面最低点恰好和环形刻度线相切;④用于稀释NaOH溶液的仪器未洗涤。
(安徽省芜湖市一中2008届高三第二次模拟考试,化学,16)下面a~e是中学化学实验中常见的几种定量仪器:
(a)量筒(b)容量瓶(c)滴定管(d)托盘天平(e)温度计
(1)其中标示出仪器使用温度的是(填写编号)
(2)由于操作错误,使得到的数据比正确数据偏小的是(填写编号)
A.实验室制乙烯测量混合液温度时,温度计的水银球与烧瓶底部接触
B.中和滴定达终点时俯视滴定管内液面读数
C.使用容量瓶配制溶液时,俯视液面定容所得溶液的浓度
(3)称取10.5g固体样品(1g以下使用游码)时,将样品放在了天平的右盘,则所称样品的实际质量为g。
Ⅰ.化学实验室制取氯化氢气体的方法之一是将浓硫酸滴入浓盐酸中。请从下图中挑选所需仪器,在方框内画出用该方法制备、收集干燥氯化氢气体的装置简图,并在图中标明所用试剂。(仪器可重复使用,固定装置不必画出)。
Ⅱ.实验室制备少量硫酸亚铁晶体的实验步骤如下:取过量洁净的铁屑,加入20%-30%的稀硫酸溶液,在50℃-80℃水浴中加热至不再产生气泡。将溶液趁热过滤,滤液移至试管中,用橡胶塞塞紧试管口,静置、冷却一段时间后收集产品。
(1)写出该实验制备硫酸亚铁的化学方程式:。
(2)硫酸溶液过稀会导致。
(3)采用水浴加热的原因是。
(4)反应时铁屑过量的目的是(用离子方程式表示)。
(5)溶液趁热过滤的原因是塞紧试管口的目的是
(6)静置冷却一段时间后,在试管中观察到的现象是。