常温下,将pH = 5的硫酸溶液稀释到原来的500倍,则稀释后溶液中c(SO42-)与c(H+)之比大约为
| A.1∶1 | B.1∶10 | C.1∶2 | D.10∶1 |
草酸是二元中强酸,草酸氢钠溶液显酸性。常温下,向10 mL 0.01 mol·L-1 NaHC2O4溶液中滴加0.01 mol·L-1 NaOH溶液,随着NaOH溶液体积的增加,溶液中离子浓度关系正确的是
| A.V(NaOH) = 0时,c(H+) = 1×10-2 mol·L-1 |
| B.V(NaOH)<10 mL时,不可能存在c(Na+) = 2c(C2O42-)+c(HC2O4- ) |
| C.V(NaOH) =" 10" mL时,c(H+) = 1×10-7 mol·L-1 |
| D.V(NaOH)>10 mL时,c(Na+)>c(C2O42-)>c(HC2O4- ) |
化合物Bilirubin在一定波长的光照射下发生分解反应,反应物尝试随反应时间变化如图所示,计算反应4~8 min间的平均反应速率和推测反应16 min 反应物的浓度,结果应是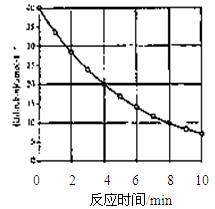
A.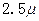 mol·L-1·min-1和 mol·L-1·min-1和 mol·L-1 mol·L-1 |
B.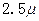 mol·L-1·min-1和 mol·L-1·min-1和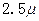 mol·L-1 mol·L-1 |
C.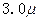 mol·L-1·min-1和 mol·L-1·min-1和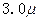 mol·L-1 mol·L-1 |
D. mol·L-1·min-1和 mol·L-1·min-1和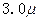 mol·L-1 mol·L-1 |
25℃时,水的 电离达到平衡:H2O
电离达到平衡:H2O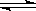 H++OH-;ΔH>0,下列叙述正确的是
H++OH-;ΔH>0,下列叙述正确的是
| A.向水中加入稀氨水,平衡逆向移动,c(OH-)降低 |
| B.向水中加入少量固体硫酸氢钠,c(H+)增大,Kw不变 |
| C.向水中加入少量固体CH3COONa,平衡逆向移动,c(H+)降低 |
| D.将水加热,Kw增大,pH不变 |
把Ca(OH)2放入蒸馏水中,一段时间后达到平衡:Ca(OH)2(s) Ca2++2OH-下列说法正确的是
Ca2++2OH-下列说法正确的是
| A.恒温下向溶液中加CaO,溶液的pH升高 |
| B.给溶液加热,溶液的pH升高 |
| C.向溶液中加入Na2CO3溶液,其中固体质量增加 |
| D.向溶液中加入少量NaOH固体,Ca(OH)2固体质量不变 |
已知一种c(H+)=1×10-3 mol·L-1的酸和一种c(OH-)=1×10-3 mol·L-1碱溶液,等体积混合后溶液呈酸性,其原因可能是
| A.浓的强酸和稀的强碱溶液反应 | B.浓的弱酸和稀的强碱溶液反应 |
| C.等浓度的弱碱和强酸溶液反应 | D.生成了一种强酸弱碱盐 |