某厂以甘蔗为原料制糖,对产生的大量甘蔗渣按下图所示转化进行综合利用。其中B是A水解的最终产物;C的化学式为C3H6O3,一定条件下2个C分子间脱去2个水分子可生成一种六元环状化合物;D可使溴水褪色。(图中部分反应条件及产物没有列出)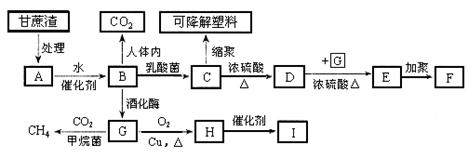
(1)写出下列物质的结构简式:
①高分子化合物F_________________;②C脱水生成的六元环状化合物的结构简式___________。
(2)写出反应G→H的化学方程式: 。
(3)写出A与浓硝酸在一定条件下的反应 ,该反应类型为 。
8分)电解原理在化学工业中有广泛应用。下图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连。请回答以下问题:
(1)若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,则
a.电解池中X极上的电极反应式为 ① 。在X极附近观察到的现象是 ②。
b.Y电极上的电极反应式为 ③ ,检验该电极反应产物的方法是④。
(2)如要用电解方法精炼粗铜,电解液a选用CuSO4溶液,则
a .X电极的材料是⑤,电极反应式是⑥。
b.Y电极的材料是⑦,电极反应式是⑧。
(说明:杂质发生的电极反应不必写出)
某研究性学习小组为证明在同温同压下,相同浓度相同体积的不同强度的一元酸与足量镁带反应时,生成氢气的体积相同而反应速率不同,同时测定实验室条件下的气体摩尔体积。设计的简易实验装置如图。
该实验的主要操作步骤如下:
a.配制浓度均为1 mol·L-1盐酸和醋酸溶液;
b.用 ① 量取10.00 mL1 mol·L-1盐酸和醋酸溶液分别加入两个锥形瓶中;
c.分别称取除去表面氧化膜的镁带a g,并系于铜丝末端,a的数值至少为 ② g;d.在广口瓶中装足量的水,按图连接好装置;检查装置的气密性;e.将铜丝向下移动,使足量镁带浸入酸中,至反应完全,记录 ③ ;
f.反应结束后待温度恢复到室温,若丙中液面高于乙中液面,读取量筒中水的体积前,应 ④ ,读出量筒中水的体积为V mL。
请将上述步骤补充完整并回答下列问题:
(1)用文字表述d检查该装置气密性的操作与观察方法: ⑤ 。
(2)本实验中应选用 ⑥ (填序号)的量筒。
A.100 mL B.200 mL C.500 mL
(3)简述速率不等的原因 ⑦ ,铜丝不与酸接触的原因是 ⑧ 。
某学生为测定未知浓度的硫酸溶液,实验如下:用1.00mL待测硫酸配制100 mL稀H2SO4溶液;以0.14mol/L的NaOH溶液滴定上述稀H2SO425.00mL,滴定终止时消耗NaOH溶液15.00mL。
(1)该学生用标准0.14 mol/L NaOH溶液滴定硫酸的实验操作如下:
| A.用酸式滴定管取稀H2SO4 25.00 mL,注入锥形瓶中,加入指示剂。 |
| B.用待测定的溶液润洗酸式滴定管。 |
| C.用蒸馏水洗干净滴定管。 |
| D.取下碱式滴定管用标准的NaOH溶液润洗后,将标准液注入碱式滴定管刻度“0”以上2~3 cm处,再把碱式滴定管固定好,调节液面至刻度“0”或“0”刻度以下。 E.检查滴定管是否漏水。 F.另取锥形瓶,再重复操作一次。 G.把锥形瓶放在滴定管下面,瓶下垫一张白纸,边滴边摇动锥形瓶直至滴定终点,记下滴定管液面所在刻度。 |
a、滴定操作的正确顺序是(用序号填写):①。
b、该滴定操作中应选用的指示剂是:②。
c、在G操作中如何确定终点?③。
(2)碱式滴定管用蒸馏水润洗后,未用标准液润洗导致滴定结果(填“偏小”、“偏大”或“恰好合适”) ④ ,原因是⑤。
(3)计算待测硫酸(稀释前的硫酸)溶液的物质的量浓度(计算结果精确到小数点后二位)⑥mol/L
下图是某化学兴趣小组设计的乙醇催化氧化的实验装置(图中加热仪器、铁架台、试管夹均未画出)。图中A处为无水乙醇(沸点78℃),B处为绕成螺旋状的细铜丝或银丝,C处为无水CuSO4粉末,D处为碱石灰,F处为新制的碱性Cu(OH)2悬浊液。
(1)在上述装置中,实验需要加热的仪器为(填序号)。
(2)为使A中乙醇平稳地汽化成乙醇蒸气,常用的方法是。
(3)若E中的固体为纯净物,则E的化学式是。
学生利用下图所列装置进行“铁与水蒸气反应”的实验,并利用产物进一步制取FeCl3·6H2O晶体。(图中夹持及尾气处理装置均已略去)
(1)回答下列问题:所用铁粉中若有杂质,欲除去不纯铁粉中混有的铝粉可以选用的试剂为(填序号)。
| A.稀盐酸 | B.氢氧化钠溶液 | C.浓硫酸 | D.FeCl3溶液 |
此步涉及反应的离子方程式为。
(2)反应发生后装置B中发生反应的化学方程式是。
D装置的作用:。
(3)该小组学生把B中反应后的产物加入足量的盐酸,过滤,用上述滤液制取FeCl3·6H2O晶体,设计流程如下:
①用离子方程式表示步骤I中通入Cl2的作用。
②为了检验某未知溶液是否是FeCl2溶液,同学们设计了以下实验方案加以证明。
向一支装有该未知溶液的试管中先通入氯气,再滴加KSCN溶液,溶液呈现红色,证明该未知溶液是FeCl2溶液。你认为此方案是否合理(填“合理”或“不合理”)。