在氯化钡溶液中通入SO2,无白色沉淀产生。若将氯化钡溶液分装在两只试管中,一支加硝酸,另一支加NaOH溶液,然后再分别通入适量的SO2,结果两支试管中都有白色沉淀生成。由此得出下列结论正确的是
| A.加入NaOH,溶液pH升高,c(SO32-)增大 |
| B.氯化钡有两性 |
| C.两支试管中的白色沉淀都是BaSO4 |
| D.SO2具有两性且水溶液有酸性 |
下列各组指定物质的同分异构体数目相等的是
| A.乙烷的二氯代物和丙烷的一氯代物 | B.丙烷的一氯代物和戊烷 |
| C.苯的二氯代物和苯的一硝基代物 | D.C3H6和C5H12 |
某烃的化学式为C4Hm,下列关于C4Hm的说法中正确的是
| A.当m=8时,该烃一定与乙烯互为同系物 |
| B.当m=4时,该烃一定含有碳碳双键 |
| C.该烃不可能同时含有碳碳双键和碳碳三键 |
| D.1mol C4Hm完全燃烧,不可能生成3.5mol H2O |
下列反应中,属于取代反应的是
①CH3CH=CH2+Br2 CH3CHBrCH2Br
CH3CHBrCH2Br
②CH3CH=CH2+Br2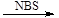 CH2BrCH=CH2+HBr
CH2BrCH=CH2+HBr
③ +HNO3
+HNO3
 +H2O
+H2O
④CH3CH2OH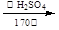 CH2=CH2↑+ H2O
CH2=CH2↑+ H2O
| A.②④ | B.③④ | C.①③ | D.②③\ |
设NA为阿伏加德罗常数的值,下列有关叙述正确的是
| A.1 mol羟基所含的电子总数为10NA |
| B.标准状况下,1L正戊烷完全燃烧所生成的CO2分子数为5NA/22.4 |
| C.4.2g乙烯和丙烯的混合气体中所含碳原子数为0.2NA |
| D.1 mol碳正离子(CH3+)所含的电子总数为8NA |
有9种物质:①甲烷②环己烷③环己烯④苯乙烯⑤聚乙烯⑥2—丁炔⑦苯⑧邻—二甲苯⑨Na2SO3溶液,其中既能使酸性KMnO4溶液褪色,又能因化学反应使溴水褪色的是
| A.③④⑥⑨ | B.③④⑥⑧ | C.③④⑤⑥⑨ | D.③④⑤⑥⑧ |