分别将下列物质:①CuSO4②Na2O2③NaCl④Ca(HCO3)2⑤FeCl3投入水中,对其溶液加热蒸干,仍能得到原物质的是
| A.①②③ | B.①③ | C.③④ | D.③ |
以下4种有机物的分子式都是C4H10O: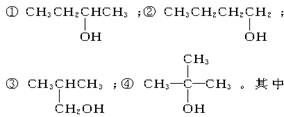
能被氧化成含相同碳原子数的醛的是()
| A.①② | B.只有② | C.②③ | D.③④ |
下列反应中,有机物被还原的是 ( )
| A.乙醛的银镜反应 | B.乙醛制乙醇 | C.乙醇制乙醛 | D.乙醇制乙烯 |
一定条件下,X(g)+3Y(g) 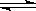 2Z(g)达到反应限度的标志是()
2Z(g)达到反应限度的标志是()
| A.Z的分解速率和生成速率相等 |
| B.X、Y、Z的浓度不再变化 |
| C.反应体系的总质量保持不变 |
| D.单位时间内生成nmolZ,同时生成nmolX |
目前含有元素硒(Se)的保健品已开始涌入市场,已知它与氧同主族,而与钙同周期,下列关于硒的有关描述中不正确的是( )
| A.原子序数24 | B.最高价氧化物为SeO2,为酸性氧化物 |
| C.原子半径比钙小 | D.气态氢化物化学式为H2Se |
金刚石和石墨都是碳的单质,石墨在一定条件下可以转化为金刚石。已知12g石墨完全转化为金刚石时,要吸收EkJ的能量,下列说法正确的是
| A.金刚石与石墨互为同位素 | B.石墨不如金刚石稳定 |
| C.金刚石不如石墨稳定 | D.等质量的石墨与金刚石完全燃烧,金刚石放出的能量多 |