有一固体混合物,可能由Na2CO3、Na2SO4、CuSO4、CaCl2、NaCl混合而成.为检验它的成分做了如下实验:①将固体混合物溶于水,搅拌后得到无色透明溶液;②往此溶液中滴加硝酸钡溶液,有白色沉淀生成;③过滤,将沉淀物置于稀硝酸中,发现沉淀全部溶解.则该固体混合物中
| A.肯定有Na2CO3,可能有CuSO4 |
B.一定有NaCl,肯定没有Na2SO4 |
| C.一定有Na2CO3,可能有NaCl | |
| D.可能有CaCl2,一定没有CuSO4 |
化合物HIn在水溶液中因存在以下电离平衡,故可用作酸碱指示剂
HIn(溶液) H+(溶液)+In-(溶液)
H+(溶液)+In-(溶液)
红色黄色
浓度为0.02 mol·L-1的下列各溶液①盐酸②石灰水③NaCl溶液④NaHSO4溶液⑤NaHCO3溶液⑥氨水,其中能使指示剂显红色的是()
| A.②⑤⑥ | B.①④ | C.①④⑤ | D.②③⑥ |
反应速率v和反应物浓度的关系是用实验方法测定的,化学反应H2+Cl2=2HCl的反应速率v可表示为v=K[c(H2)]m[c(Cl2)]n,式中K为常数,m、n的值可用下表中的数据确定。
| c(H2)(mol·L-1) |
c(Cl2)(mol·L-1) |
v(mol·L-1·s-1) |
| 1.0 |
1.0 |
1.0K |
| 2.0 |
1.0 |
2.0K |
| 2.0 |
4.0 |
4.0K |
由此可推得m、n的值正确的是()
A. m=1,n=1 B. m=1/2,n=1/2 C. m=1/2,n=1 D. m=1,n=1/2
人体血液内的血红蛋白(Hb)易与O2结合生成HbO2, 因此具有输氧能力,CO吸入肺中发生反应:CO+HbO2 O2+HbCO,37 ℃时,该反应的平衡常数K=220。HbCO的浓度达到HbO2浓度的0.02倍,会使人智力受损。据此,下列结论错误的是()
O2+HbCO,37 ℃时,该反应的平衡常数K=220。HbCO的浓度达到HbO2浓度的0.02倍,会使人智力受损。据此,下列结论错误的是()
A.CO与HbO2反应的平衡常数K= |
| B.人体吸入的CO越多,与血红蛋白结合的O2越少 |
| C.当吸入的CO与O2浓度之比大于或等于0.02时,人的智力才会受损 |
| D.把CO中毒的病人放入高压氧仓中解毒,其原理是使上述平衡向左移动 |
乙酸乙酯能在多种条件下发生水解反应:
CH3COOC2H5+H2O CH3COOH+C2H5OH。
CH3COOH+C2H5OH。
已知该反应的速率随c(H+)的增大而加快。下图为CH3COOC2H5的水解速率随时间的变化如图。下列说法中正确的是()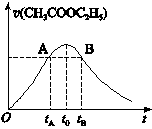
A.反应初期水解速率增大可能是溶液中c(H+)增大所致
B.A、B两点表示的c(CH3COOC2H5)相等
C.图中t 0时反应达到平衡状态
D.t 0时CH3COOC2H5的转化率低于tA时CH3COOC2H5的转化率
一定条件下,下列反应中水蒸气含量随反应时间的变化趋势符合下图的是( )

温度(T)的影响 压强(p)的影响
A.CO2(g)+2NH3(g)  CO(NH2)2(s) + H2O(g);△H<0 CO(NH2)2(s) + H2O(g);△H<0 |
B.CO2(g)+ H2(g)  CO(g) + H2O(g);△H>0 CO(g) + H2O(g);△H>0 |
C.CH3CH2OH(g)  CH2=CH2(g) + H2O(g);△H>0 CH2=CH2(g) + H2O(g);△H>0 |
D.2C6H5CH2CH3(g) + O2(g ) 2C6H5CH=CH2(g) + 2 H2O(g);△H<0 2C6H5CH=CH2(g) + 2 H2O(g);△H<0 |