已知25℃时,AgI饱和溶液中c(Ag+)为1.23×10-8mol/L,AgCl的饱和溶液中c(Ag+)为1.25×10-5mol/L。若在5mL含有KCI和KI各为0.01 mol/L的溶液中,加入8mL 0.01 mol/L AgNO3溶液,下列叙述正确是 ( )
A.混合溶液中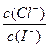 约为1.02×103 约为1.02×103 |
| B.加入AgNO3溶液时首先生成AgCl沉淀 |
| C.混合溶液中c(K+)>c(NO3-)>c(Cl-)>c(Ag+)>c(I-) |
| D.混合溶液中c(K+)>c(NO3-)>c(Ag+)>c(Cl-)>c(I-) |
污水处理的主要方法有:①中和法;②化学沉淀法;③氧化还原法;④过滤法,其中属于化学方法的是( )
| A.①②③ | B.①②④ |
| C.②③④ | D.①②③④ |
自来水厂常用氯气对生活用水进行杀菌消毒,又知氯气与水反应的产物之一是盐酸。市场上有些不法商贩为牟取暴利,用这样的自来水冒充纯净水(离子的浓度非常低)出售,给人们的生活造成了一定的不良影响。在下列化学试剂中,可以用于鉴别这种自来水和纯净水的是( )
| A.酚酞试液 | B.氯化钡溶液 |
| C.氢氧化钠溶液 | D.硝酸银溶液 |
明矾是一种较好的净水剂,这是因为( )
| A.本身有较强的吸附性 |
| B.本身与悬浮杂质生成沉淀 |
| C.Al3+水解呈酸性 |
| D.Al3+水解生成的Al(OH)3胶体有吸附作用 |
下列关于药物的使用说法正确的是()
| A.虽然药物能治病,但大部分药物有毒副作用 |
| B.使用青霉素时,不用进行试验,直接静脉注射 |
| C.长期大量使用阿司匹林可预防疾病,没有副作用 |
| D.我们生病了都可以到药店自己买药吃,不用到医院 |
在第二次世界大战中,抗生素()拯救了成千上万士兵的生命,当时被誉为与原子弹、雷达齐名的三大发明之一。
| A.青霉素 | B.阿司匹林 | C.红霉素 | D.吗啡 |